Få tillgång till LCAL2003: Chemistry labs (ultraconcurrent) nu
För endast:
9,99 US$En betalning
6 månaders åtkomst
Betalningsmetoder som stöds:
- DigiKey (Inte tillgänglig i alla länder)
- Kredit- eller betalkort
- PayPal
Du behöver skapa eller använda ett LabsLand-konto för att fortsätta.
Fjärråtkomst till 12 laboratorier ingår:
Försöker du köpa flera licenser för en klass? Kontakta oss för mängdrabatter
Vad är LabsLand?
LabsLand är det globala nätverket av fjärrlaboratorier.
Utrustningen är alltid riktig, inte en simulering.
Du styr den riktiga utrustningen med webbkameror via Internet.
Få tillgång nu. Ingen anledning att vänta på att utrustning ska skickas.
Inga dolda kostnader: allt ingår. Inga tillbehör eller fraktkostnader.
Mycket lätt att använda: utrustningen fungerar redan.
Hyra det bara de månader du behöver för ditt lärande.
Hur fungerar LabsLand?
LabsLand är ett globalt nätverk av verkliga laboratorier som finns tillgängliga online. Studenter (i skolor, universitet och livslånga lärandeplattformar) kan få tillgång till de verkliga laboratorierna via Internet med hjälp av sin bärbara dator, surfplatta eller telefon.
Laboratorierna är antingen i realtid (Arduino, FPGA:er...) och ligger i olika universitet över hela världen. Inom vissa områden (fysik, biologi, kemi) är laboratorierna LabsLand Ultrakonkurrerande laboratorier, så universitetet har spelat in alla potentiella kombinationer av vad som kan göras i laboratoriet (i vissa fall flera tusen) och gjort det tillgängligt på ett interaktivt sätt.
I varje fall är laboratoriet alltid verkligt (inte simulerat) och tillgängligt via webben (du behöver inte skaffa någon hårdvara, hantera frakt osv.).
Se hur en typisk användarsession fungerar i följande video:
Syra-bas titrering II
Sammanfattning
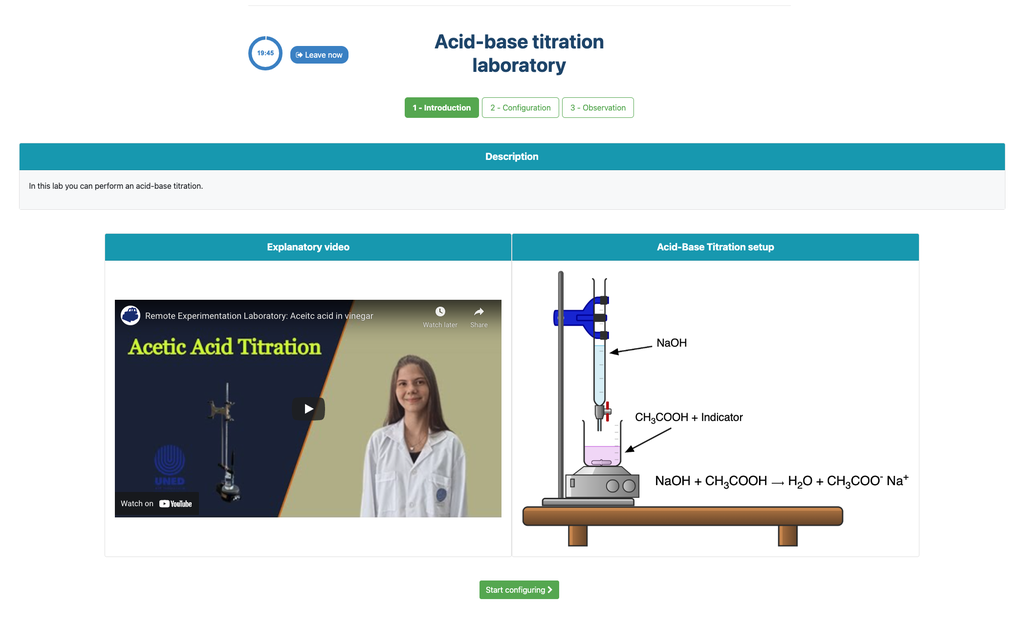
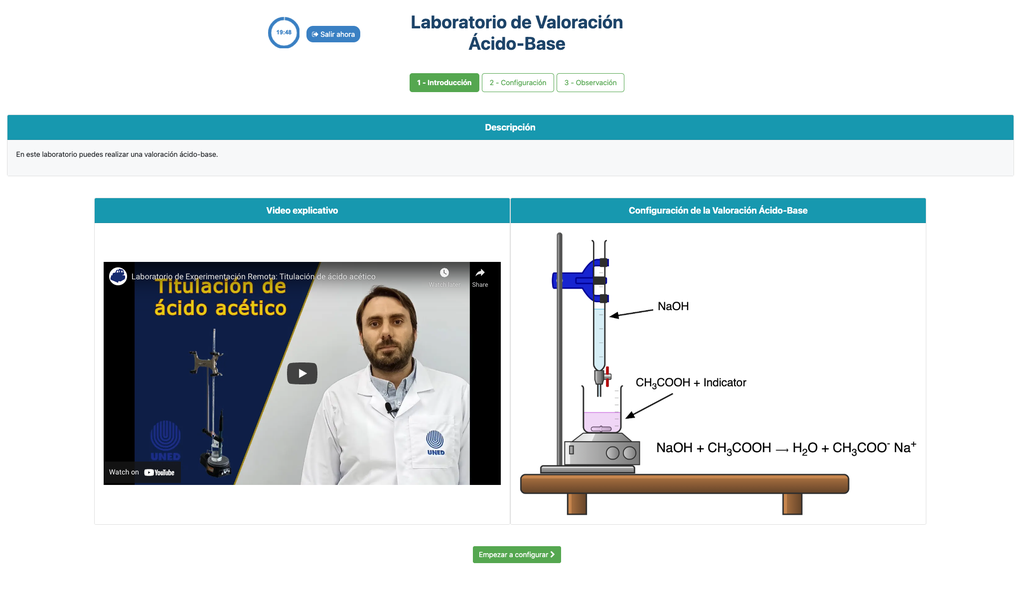
Utför en syra-bas titrering för att bestämma koncentrationen av en okänd ättiksyrelösning med hjälp av en natriumhydroxidtitrator. Detta laboratorium betonar visuella mätningar som handlar om byrettens menisk och stöder två olika konfigurationer.
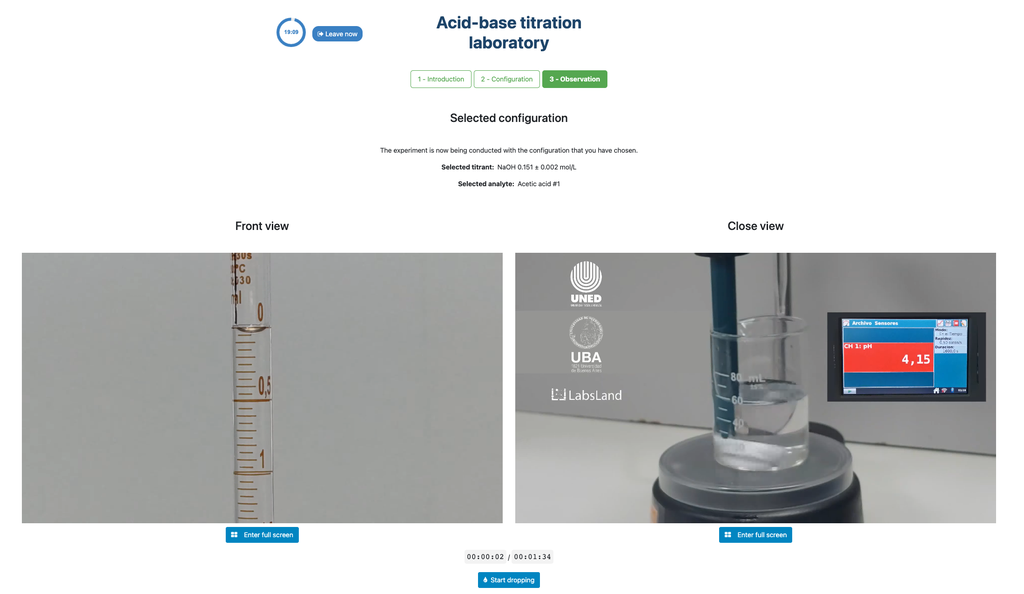
Den första är för en potentiometrisk metod: du kommer att ha tillgång till en digital pH-sensor och du kan använda den för att bestämma när den okända lösningen har neutraliserats.
Den andra är för en kolorimetrisk metod: du kan förlita dig på färgförändringen orsakad av närvaron av en fenolftaleinindikator, utan att ha en digital pH-sensor tillgänglig.
Syra-bas Titrering
Titreringar är en volymetrisk metod som baseras på att mäta mängden av ett reaktivt ämne med känd koncentration (kallad primär standard) som förbrukas av ett prov med okänd koncentration, kallad analysat.
Titreringen utförs genom att tillsätta titratorn till analysatet med hjälp av en byrett för att erhålla en kemiskt ekvivalent substans mellan titratorn och analysatet. Detta kallas "ekvivalenspunkt" och det är ett teoretiskt värde som inte kan bestämmas experimentellt.
Den experimentella uppskattningen av denna punkt erhålls genom en approximation känd som "slutpunkt". Denna bestäms genom en fysisk förändring. I det fallet uppnås färgförändringen i lösningen efter att ha tillsatt en indikatorsubstans: en substans som ändrar färg inom vissa pH-intervall.
För syra-bas titreringen använder vi en fenolftaleinindikator som blir ljusrosa efter ett pH på runt 8.4, vilket är ett värde som är mycket nära ekvivalenspunkten i de vanligaste syra-bas titreringarna.
Alternativt kan en digital pH-sensor användas för att bestämma "ekvivalenspunkt" i den potentiometriska konfigurationen.
Kolorimetrisk vs potentiometrisk metod
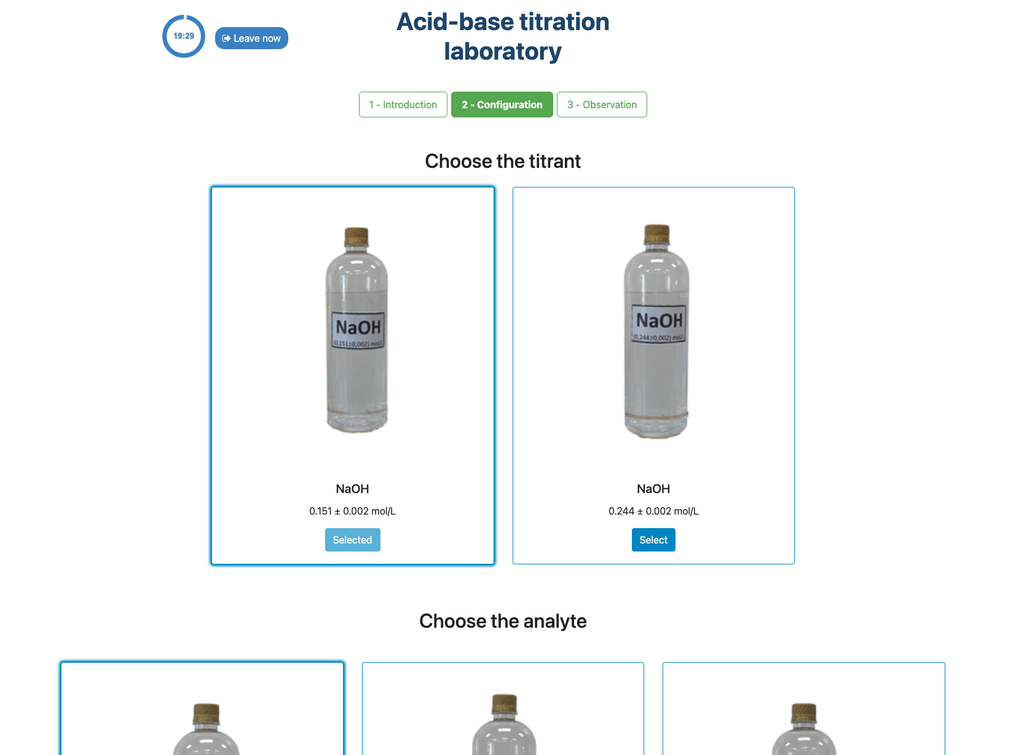
Den kolorimetriska metoden förlitar sig på färgförändringen som fenolftaleinindikatorn ger. Den potentiometriska metoden förlitar sig istället på pH-höjningen som mäts med den digitala sensorn. I denna version av laboratoriet finns två olika konfigurationer tillgängliga, en för varje metod. I den kolorimetriska konfigurationen kanske eleverna inte ser den digitala pH-sensorn.
Skillnader med laboratoriet för syra-bas titrering II
I denna version av laboratoriet (Syra-Bas Titrering II) kan du utföra syra-bas titreringen för en okänd ättiksyrelösning. I den andra versionen av laboratoriet (se Syra-Bas Titrering I) kan du utföra syra-bas titreringen för en citronsyrelösning istället.
Denna version av laboratoriet betonar visuella byrettmätningar, inklusive att korrekt läsa av menisken i byretten. Den andra versionen av laboratoriet (se Syra-Bas Titrering I) betonar inte detta och fokuserar istället på beräkningarna.
Även i denna version kan du välja mellan två olika konfigurationer: en för den potentiometriska metoden och en för den kolorimetriska metoden. Konfigurationen för den kolorimetriska metoden visar inte pH-sensorn. I den andra versionen av laboratoriet (se Syra-Bas Titrering I) finns det en enda konfiguration och sensorn visas alltid.
Syra-bas titrering III
Sammanfattning
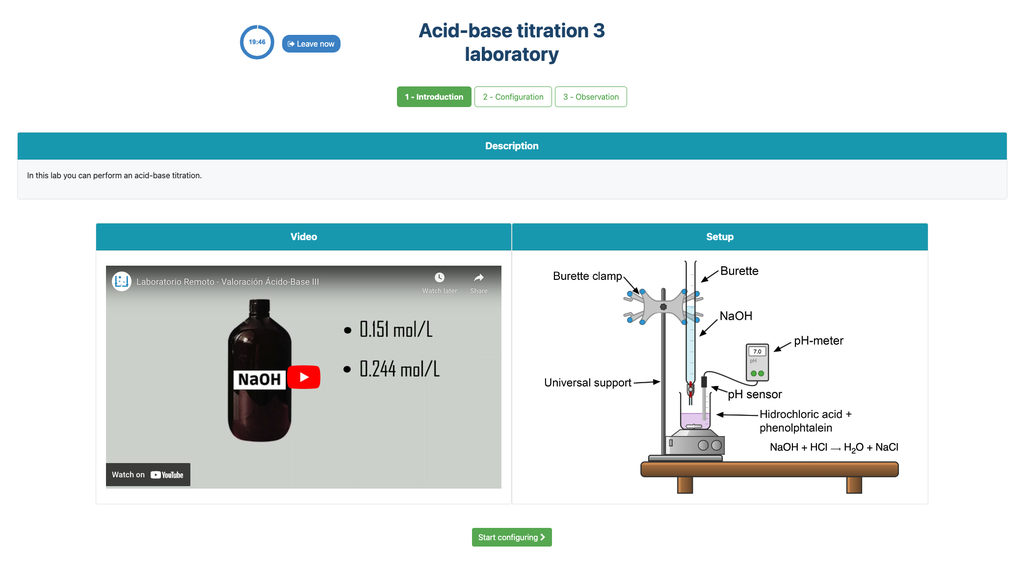
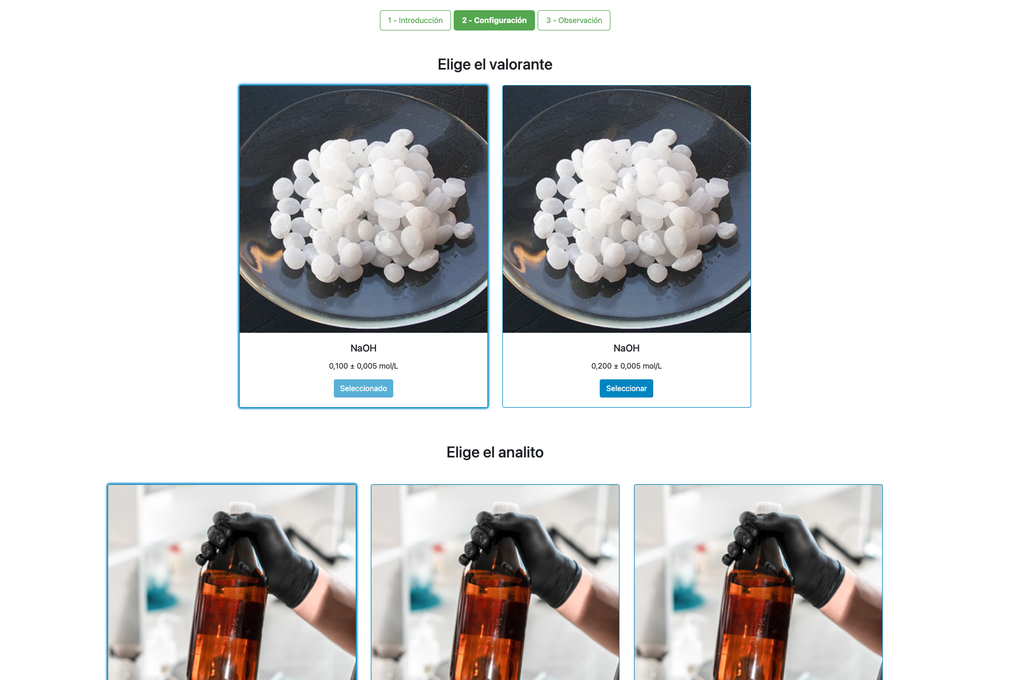
Utför en syra-bas titrering för att bestämma koncentrationen av en okänd saltsyrelösning med en natriumhydroxid titrator. Detta laboratorium betonar visuella mätningar som handlar om byrettens menisk och stöder två olika konfigurationer.
Den första är för ett potentiometriskt tillvägagångssätt: du kommer ha tillgång till en digital pH-sensor och kan använda den för att fastställa när den okända lösningen har neutraliserats.
Det andra är för ett kolorimetriskt tillvägagångssätt: du kan förlita dig på färgförändringen som sker på grund av närvaron av en fenolftaleinindikator, utan att ha en digital pH-sensor tillgänglig.
Syra-bas Titrering
Titreringar är en volymetrisk metod som bygger på att mäta mängden av ett känt-koncentrations reaktivt ämne (känd som primärstandard) som konsumeras av ett okänt-koncentrations prov känt som analysat.
Titreringen genomförs genom att tillsätta titratorn till analysatet med hjälp av en byrett för att erhålla en kemiskt-ekvivalent substans mellan titratorn och analysatet. Detta kallas för "ekvivalenspunkten" och det är ett teoretiskt värde som inte kan bestämmas experimentellt.
Den experimentella uppskattningen av denna punkt erhålls genom en approximation känd som "slutpunkt". Detta bestäms genom en fysisk förändring. I detta fall, uppnås färgförändringen av lösningen efter tillsats av en indikator substans: en substans som ändrar färg inom vissa pH-områden.
För syra-bas titreringen använder vi en fenolftaleinindikator som blir lätt rosa efter ett pH runt 8,4, vilket är ett värde mycket nära ekvivalenspunkten i de vanligaste syra-bas titreringarna.
Alternativt, i den potentiometriska konfigurationen, kan en digital pH-sensor användas för att bestämma "ekvivalenspunkten".
Kolorimetriskt vs Potentiometriskt tillvägagångssätt
Det kolorimetriska tillvägagångssättet bygger på färgförändringen som tillhandahålls av fenolftaleinindikatorn. Det potentiometriska tillvägagångssättet bygger istället på pH-förhöjningen som mäts av den digitala sensorn. I denna version av laboratoriet finns två olika tillgängliga konfigurationer, en för varje tillvägagångssätt. I den kolorimetriska konfigurationen kan studenterna kanske inte se den digitala pH-sensorn.
Skillnader med andra titreringslaboratorier
I denna version av laboratoriet (Syra-Bas Titrering II) kan du utföra syra-bas titrering för en okänd saltsyrelösning. I andra versioner av laboratoriet kan du utföra syra-bas titrering för en citronsyralösning istället (Syra-Bas Titrering I) och ättiksyra (Syra-Bas Titrering II).
Både denna version av laboratoriet (Syra-Bas Titrering III) och Syra-Bas Titrering II betonar visuella byrettmätningar, inklusive att korrekt läsa av menisken i byretten. Den andra versionen av laboratoriet (se Syra-Bas Titrering I) betonar inte detta, utan fokuserar istället på beräkningarna.
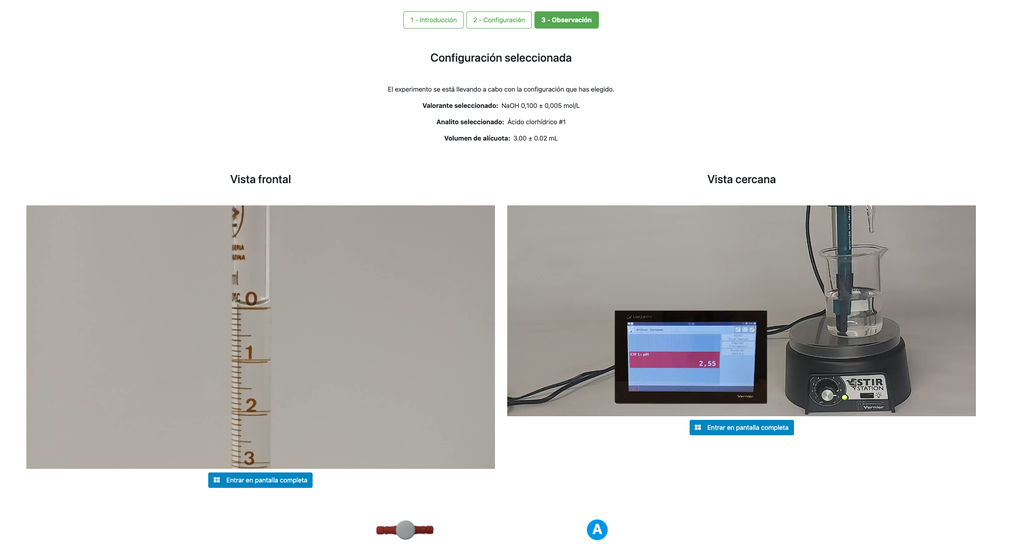
Även i dessa versioner kan du välja mellan två olika konfigurationer: en för det potentiometriska tillvägagångssättet och en för det kolorimetriska tillvägagångssättet. Konfigurationen för det kolorimetriska tillvägagångssättet visar inte pH-sensorn. I en annan version av laboratoriet (se Syra-Bas Titrering I) finns endast en konfiguration och sensorn visas alltid.

Syrabas titrering I
Sammanfattning
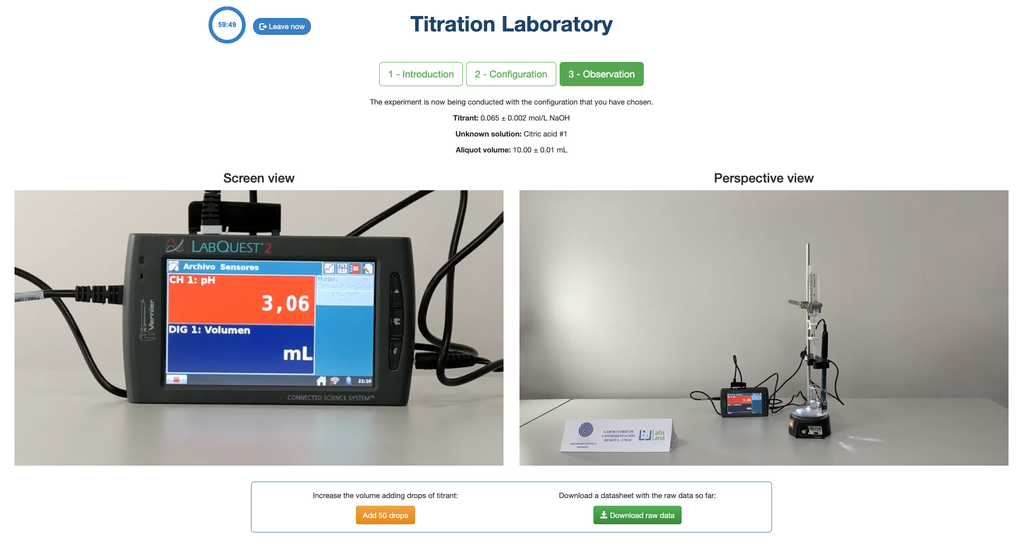
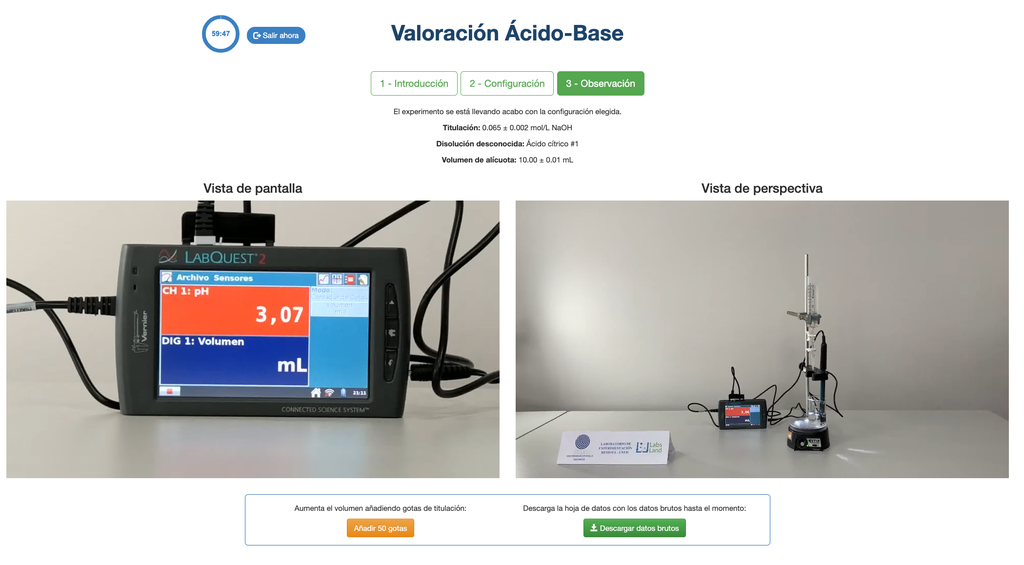
Utför en syra-bas titrering för att bestämma koncentrationen av en okänd citronsyralösning med hjälp av en natriumhydroxid-titrator. En digital pH-sensor är alltid tillgänglig och en fenolftaleinindikator har applicerats på den okända lösningen så att både en potentiometrisk och kolorimetrisk metod kan användas. Ett realtidsdiagram är också tillgängligt.
Syra-Bas Titrering
Titreringar är en volymetrisk metod som bygger på att mäta mängden av en reaktiv substans med känd koncentration (känd som en primär standard) som konsumeras av ett prov med okänd koncentration, känt som analyten.
Titreringen utförs genom att tillsätta titratorn till analyten med hjälp av en byrett, så att man får en kemiskt-ekvivalent substans mellan titratorn och analyten. Detta är känt som "ekvivalenspunkten" och det är ett teoretiskt värde som inte kan bestämmas experimentellt.
Den experimentella uppskattningen av denna punkt fås genom en approximation känd som "slutpunkt". Denna bestäms genom en fysisk förändring. I detta fall uppnås färgförändringen av lösningen efter tillsättning av en indikator: en substans som ändrar färg inom vissa pH-intervall.
För syra-bas titrering använder vi en fenolftaleinindikator som blir ljusrosa efter ett pH runt 8,4, vilket är ett värde som ligger mycket nära ekvivalenspunkten i de vanligaste syra-bas titreringarna.
Kolorimetriska vs Potentiometriska metoder
Den kolorimetriska metoden förlitar sig på färgförändringen orsakad av fenolftaleinindikatorn. Den potentiometriska metoden förlitar sig istället på pH-förhöjningen som mäts av den digitala sensorn. I denna version av syra-bas titreringslaboratoriet kan båda metoderna användas. Den digitala sensorn är alltid tillgänglig och kan inte döljas.
Skillnader med laboratoriet för Syra-Bas Titrering II
I denna version av laboratoriet (Syra-Bas Titrering I) kan du utföra syra-bas titrering för en okänd citronsyralösning. I den andra versionen av laboratoriet (se Syra-Bas Titrering II) kan du istället utföra titrering för en ättiksyrelösning.
Denna version av laboratoriet betonar beräkningarna men har inte visuella byrettmätningar bland sina lärandemål. Den andra versionen av laboratoriet (se Syra-Bas Titrering II) betonar visuella mätningar, och studenterna måste lära sig att läsa av menisken i byretten på rätt sätt.
Även i denna version finns en enda erfarenhet som kan användas för både den kolorimetriska och potentiometriska metoden. I den andra versionen av laboratoriet (se Syra-Bas Titrering II) finns två olika konfigurationer tillgängliga, varav i en döljs den digitala sensorn så att studenterna endast kan förlita sig på färgförändringen.
Boyles lag
Sammanfattning
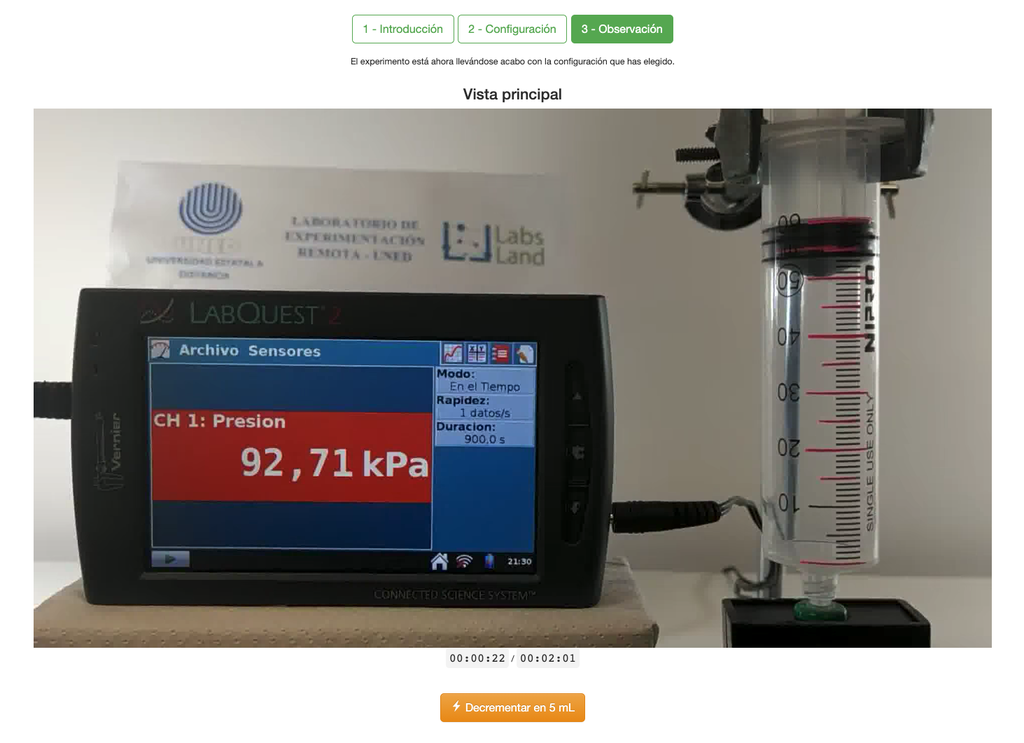
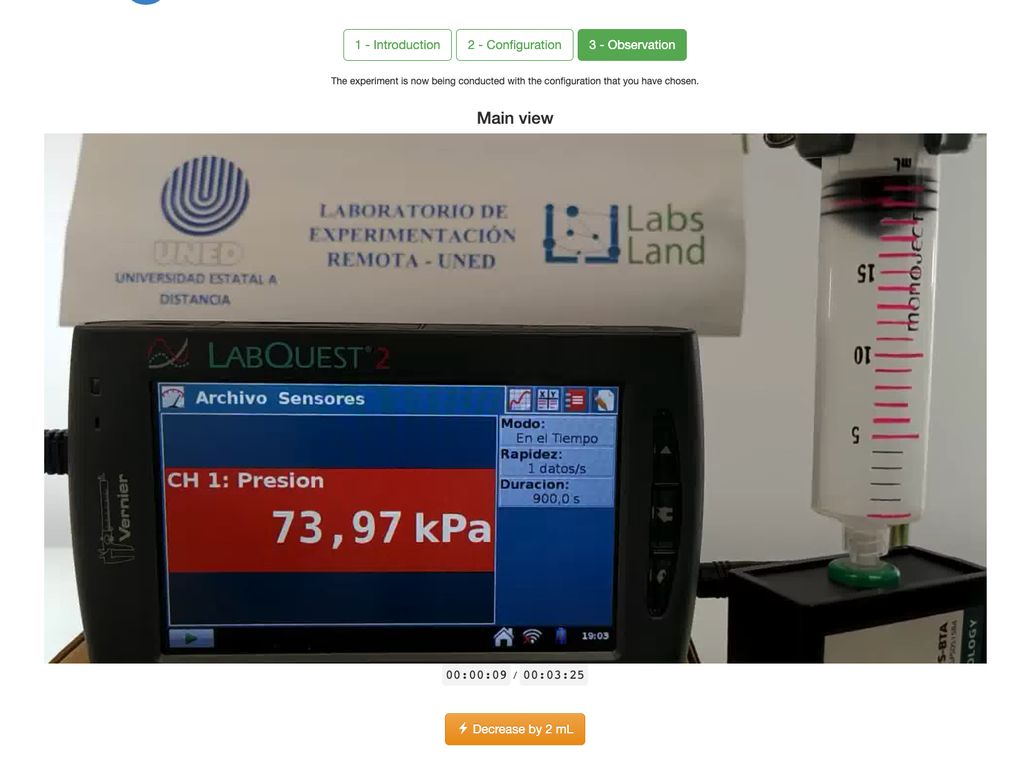
Boyles lag-laboratoriet gör det möjligt för elever att bestämma förhållandet mellan trycket och volymen av en gas vid omgivande och konstant temperatur. Eleverna kan välja mellan två olika volymsprutor och mäta gasens tryck när de minskar volymen. Experimentet återspeglas i en grafisk analys i form av en isoterm. På så sätt kan de verifiera Boyles lag och lära sig om gasernas beteende på ett praktiskt och tillgängligt sätt.
Boyles lag
Boyles lag säger att vid konstant temperatur är volymen av en gas omvänt proportionell mot dess tryck. Detta innebär att när trycket på en gas ökar minskar dess volym, och vice versa. Boyles lag kan matematiskt uttryckas som:
V
Där V är gasens volym och P är gasens tryck.
Boyles lag-laboratoriet gör det möjligt för elever att sätta denna lag i praktiken och verifiera den i en experimentell kontext. Genom att mäta volymen och trycket på gasen vid olika tidpunkter kan de rita en isoterm graf som visar hur gasens volym ändras beroende på dess tryck. Om isoterma grafen passar Boyles lag, har eleverna experimentellt verifierat lagen.
Att genomföra experiment som detta är ett utmärkt sätt att lära sig om gasers beteende och hur olika variabler är relaterade. Dessutom kan praktiska experiment vara mer tillgängliga och minnesvärda för eleverna än att bara läsa om lagen i en lärobok. Isoterma grafen visualiserar tydligt gasens beteende och verifierar om förutsägelserna av Boyles lag uppfylls.
Tillämpning i gymnasie- och universitetsutbildning
Boyles lag-laboratoriet tillämpas vanligtvis i naturvetenskapskurser på gymnasienivå och i kemikurser på universitetsnivå. På gymnasienivå kan laboratoriet tillämpas i en naturvetenskapskurs där basala koncept för kemi och fysik, såsom tryck och volym av gaser, studeras. På universitetet kan Boyles lag-laboratoriet tillämpas i en mer avancerad kemikurs där studiet av gaser och deras beteende fördjupas.
Syften
Ett Boyles lag-laboratorium kan ha olika pedagogiska syften beroende på utbildningsnivån vid vilken den tillämpas. Här är några exempel på syften som ett Boyles lag-laboratorium kan ha på både gymnasie- och universitetsnivå:
På gymnasienivå:
- Eleverna förstår Boyles lag och dess betydelse i gasfysik.
- Eleverna övar på experimentella och observationella färdigheter.
- Eleverna utvecklar färdigheter i dataanalys och representation.
- Eleverna förstår sambandet mellan temperatur, tryck och volym av gaser.
På universitetsnivå:
- Studenter känner till Boyles lag och dess betydelse i gasfysik.
- Studenterna visar experimentella och observationella färdigheter i laboratoriet.
- Studenterna tillämpar teoretiska koncept av gasfysik i praktiska situationer.
- Studenterna utvecklar färdigheter i dataanalys och representation i en vetenskaplig kontext.
- Studenterna förstår hur temperatur, tryck och volym av gaser relaterar i olika situationer.
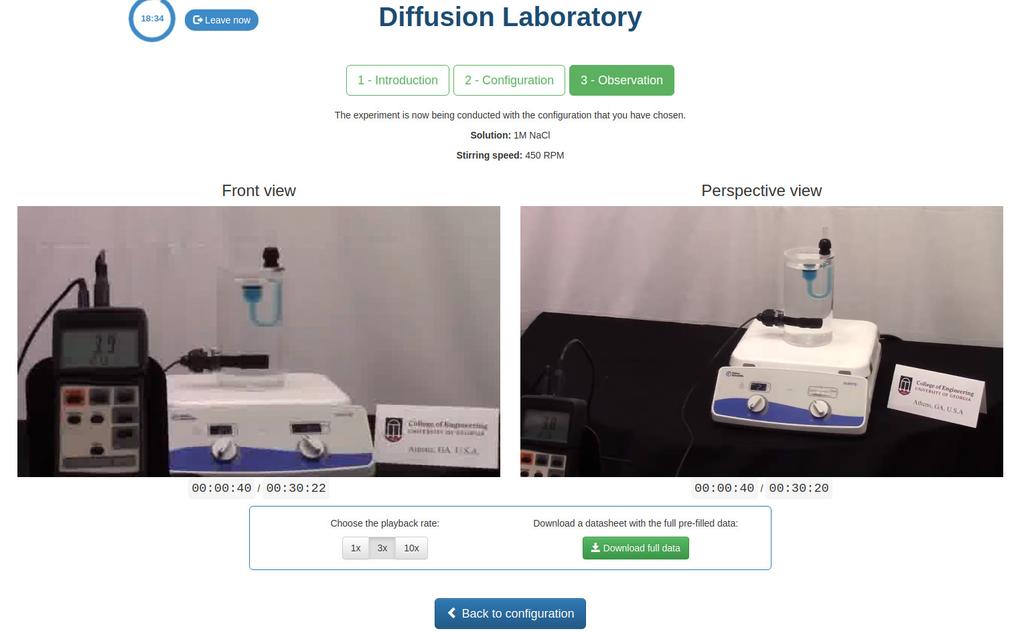
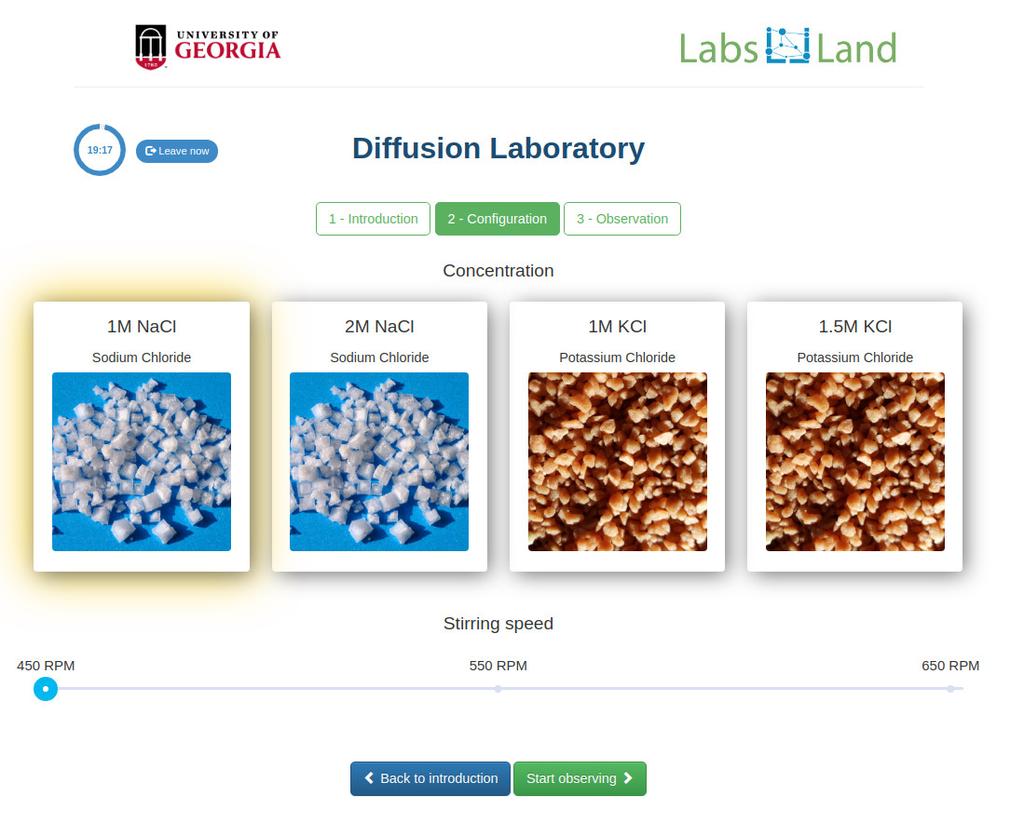
Diffusion laboratory - basic
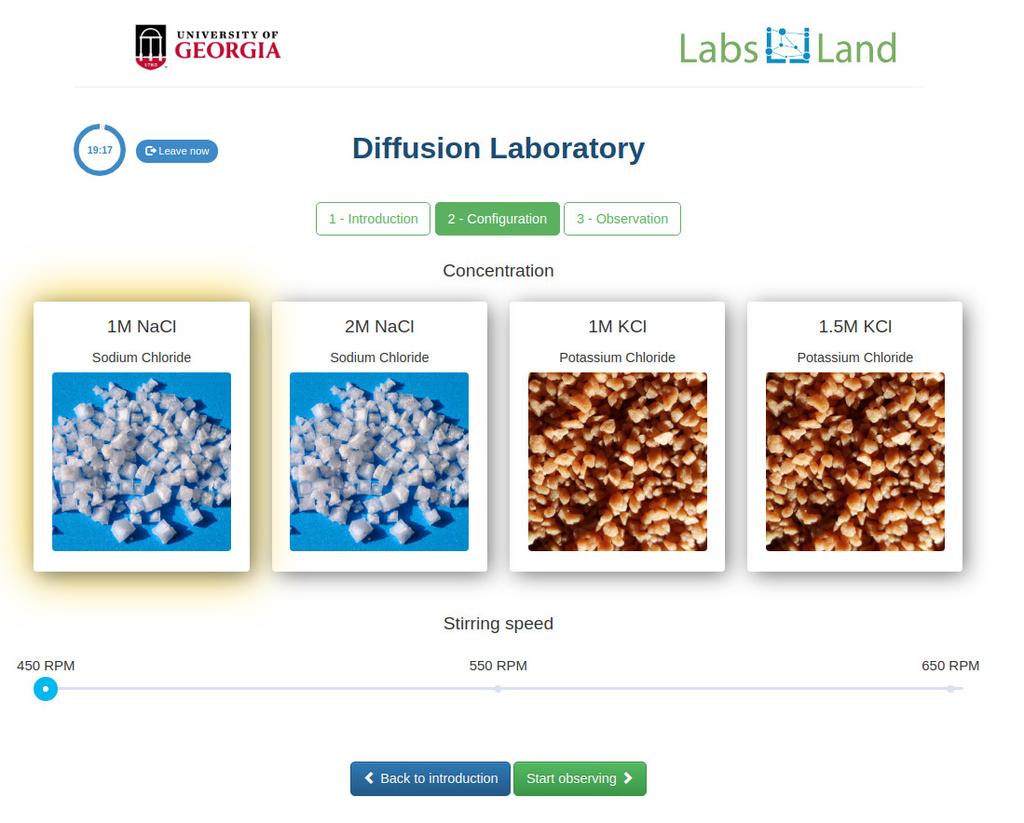
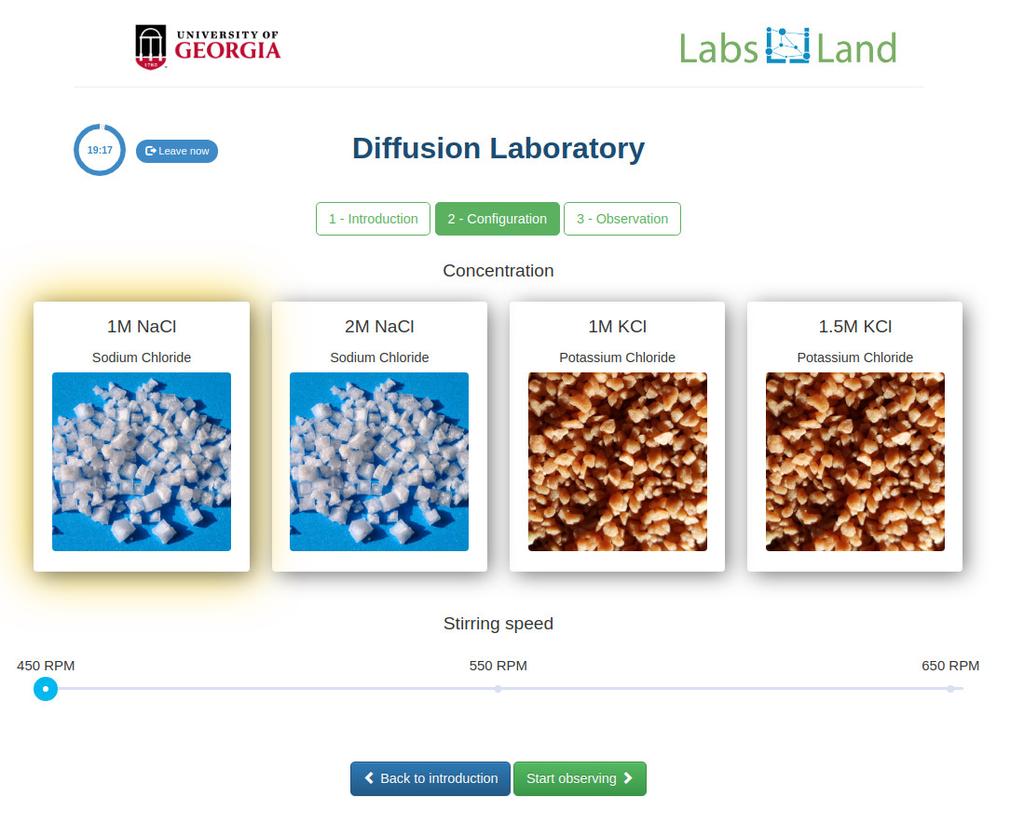
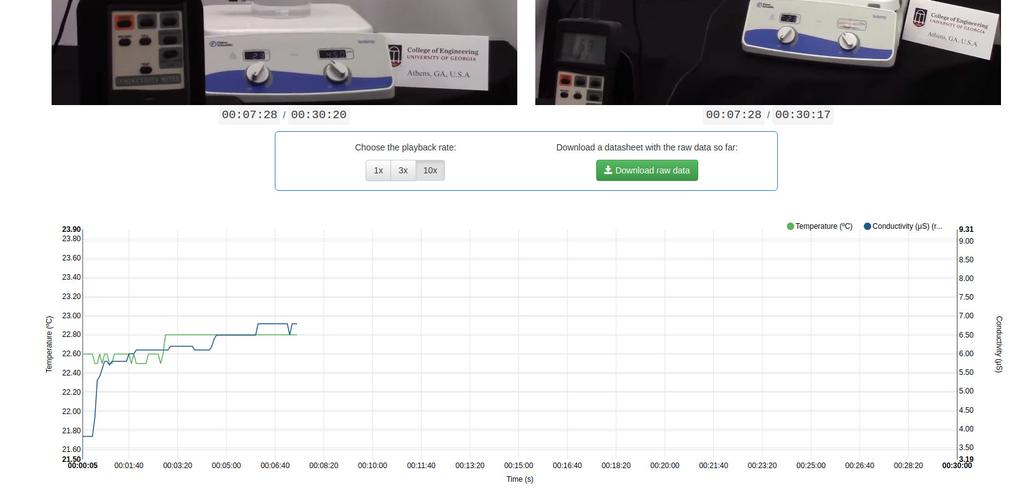
Diffusion laboratory - data
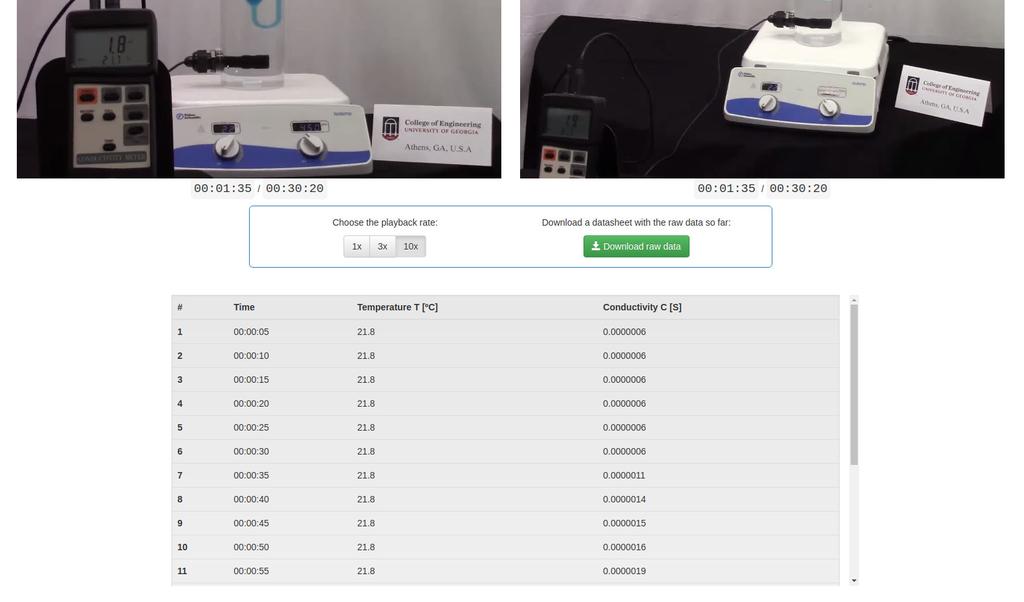
Diffusion laboratory - full
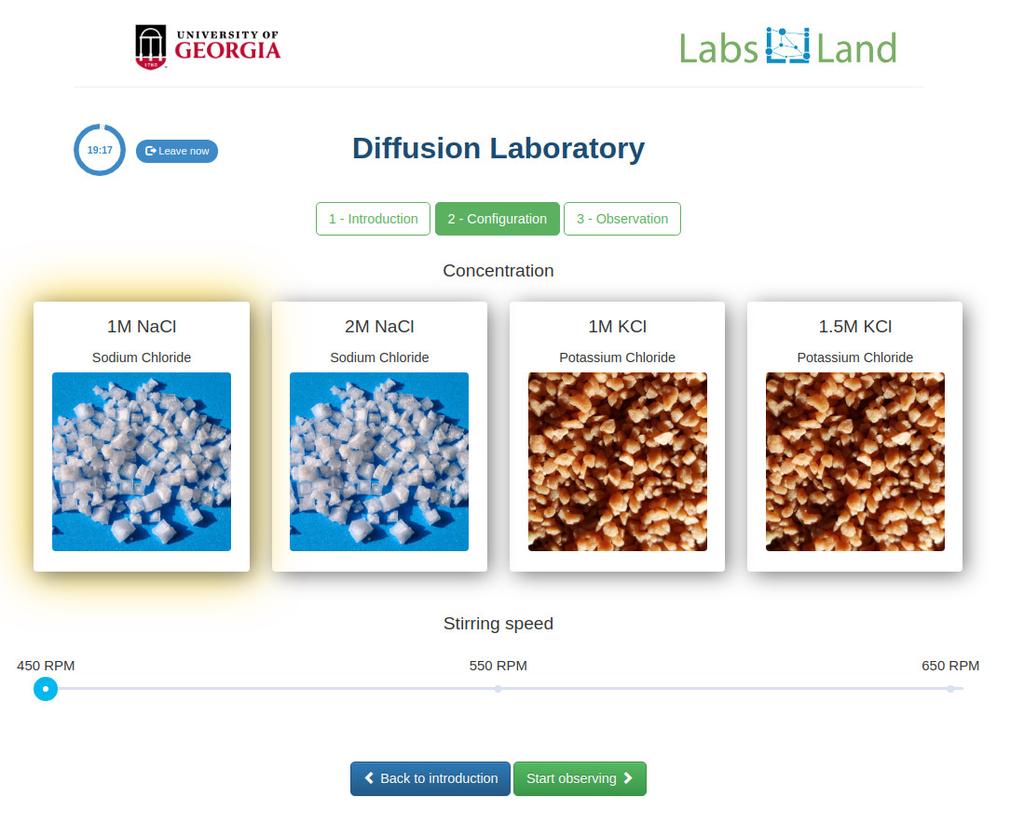
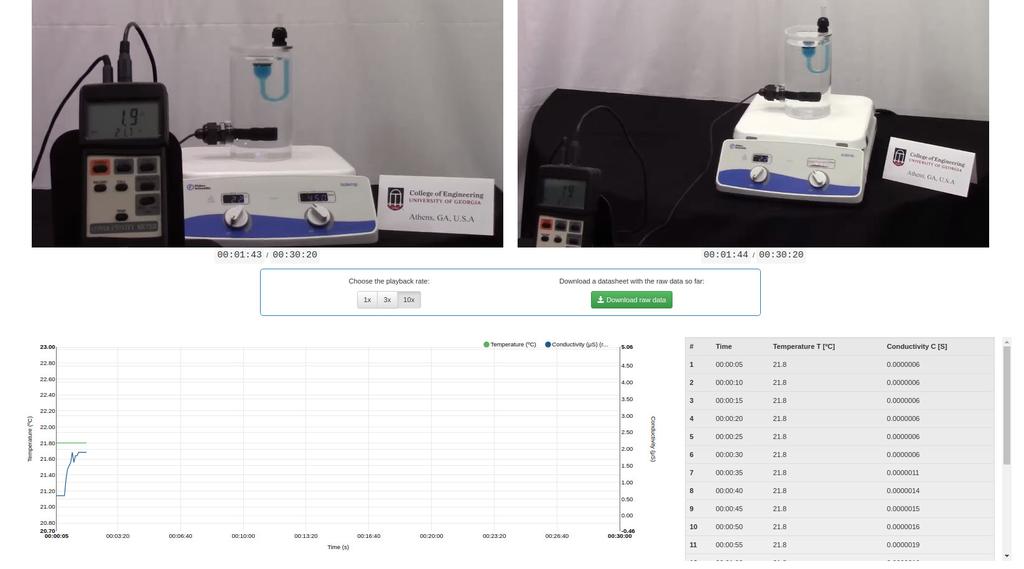
Diffusion laboratory - plot
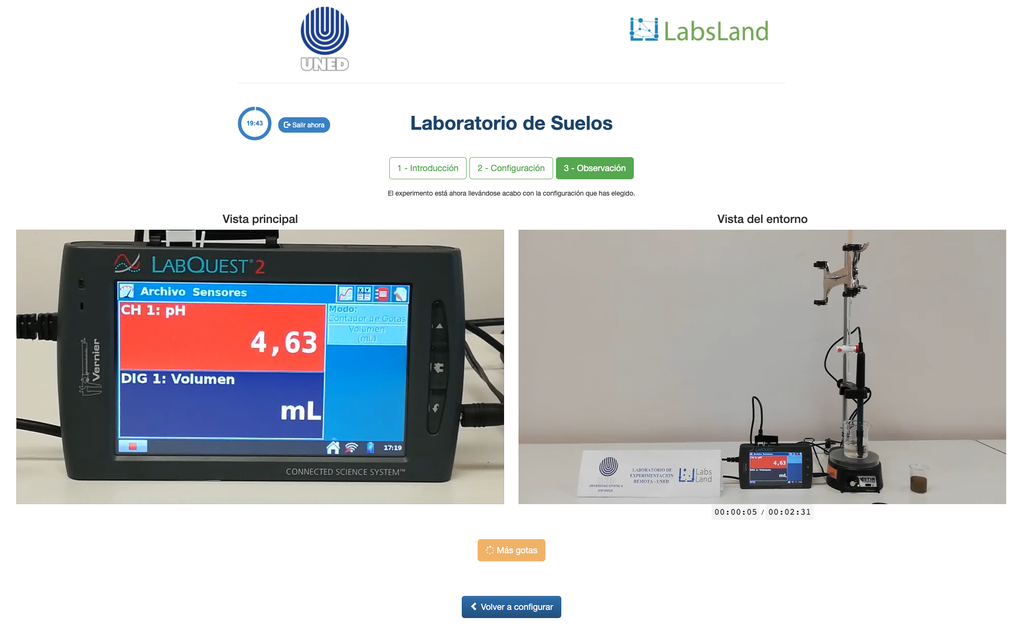
Utbytbar syrahalt i jord
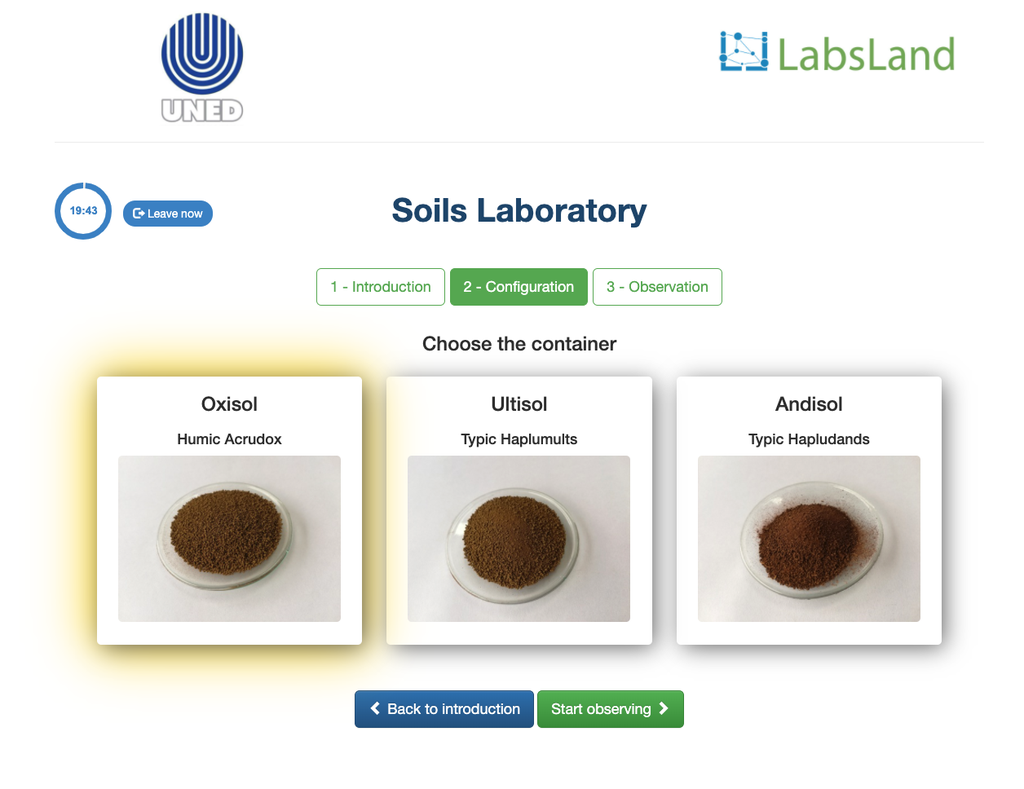
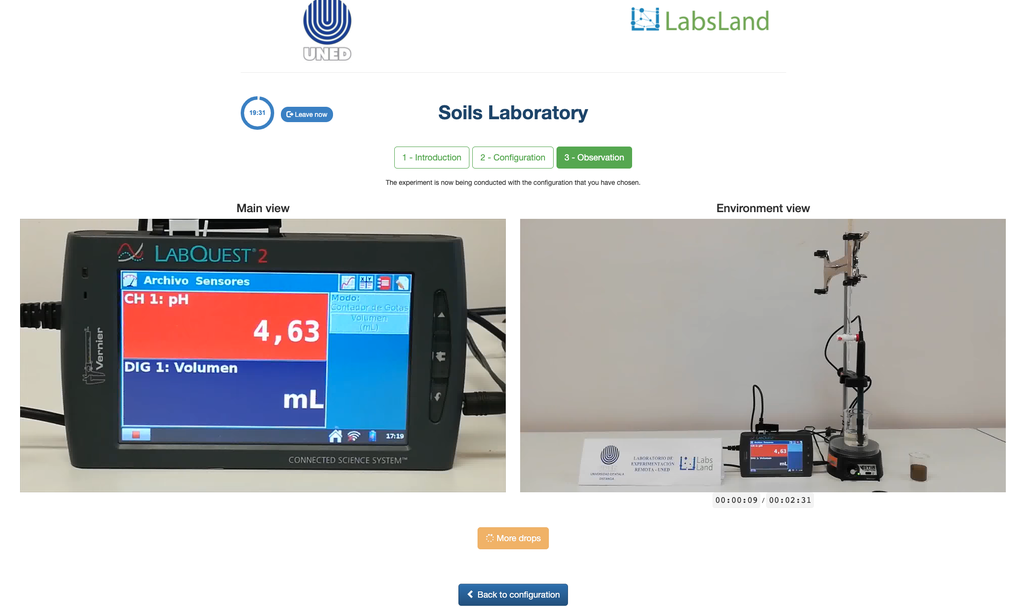
Markens surhet kan uppstå på grund av olika processer som främjar en pH-reduktion. Dessa processer sker naturligt eller genom mänsklig påverkan. De främsta källorna till markens surhet är associerade med vätejoner (H+) och aluminiumjoner (Al+3) i marklösningen. Utbytbar surhet bestäms genom användning av neutrala saltlösningar som kaliumklorid (KCl). De sura jonerna (aluminium och hydronium) som hålls i den kolloidala fraktionen av jorden, som i närvaro av en förflyttande jon (K+), får dem att komma in i marklösningen. Därefter titreras den lösningen med en natriumhydroxidlösning av exakt koncentration för att nå den sista punkten av neutraliseringsreaktionen med fenolftalein som indikator.

Gay-Lussacs lag
Gay-Lussacs lag gör det möjligt för oss att studera gasernas beteende och studeras ofta i fysik och kemi. Den relaterar gasens tryck med dess temperatur, medan andra parametrar som volym och mängd förblir konstant.
Det finns olika sätt att verifiera Gay-Lussacs lag. I detta experiment kommer vi att verifiera att för en given mängd av gasen är trycket direkt proportionellt mot temperaturen.
Radioaktivitet
Sammanfattning
Upplägget, som är användbart för skolor och universitet, inkluderar en Geiger-mätare som kan mäta antalet detekterade partikelsammanstötningar. Användaren kan välja mellan olika radioaktiva källor samt en absorberare att placera mellan den radioaktiva källan och sonden. Dessutom är andra parametrar som användare kan variera avståndet och antalet tester. Detta möjliggör en mängd olika experiment och lärandemöjligheter.
Radioaktivitet
Radioaktivitet är processen där en atomkärna förlorar energi genom att avge partiklar och strålning. Detta kan ske naturligt i vissa grundämnen, eller artificiellt genom användning av kärnreaktioner. I fysiksammanhang på skolor och universitet kan studiet av radioaktivitet ge värdefulla insikter i materiens grundläggande natur och fysikens lagar.
Ett vanligt experiment inom detta område är mätning av radioaktivitet med en Geiger-mätare. Detta instrument kan upptäcka utsläpp av partiklar från en radioaktiv källa, vilket tillåter studenter att förstå de grundläggande principerna för strålning och dess effekter på materia. Genom att variera typen av radioaktiv källa, avståndet mellan källan och detektorn, och typen av absorbermaterial placerat mellan dem, kan studenter utforska en mängd fenomen och få en djupare förståelse för de underliggande principerna.
Utöver sitt utbildningsvärde har studier av radioaktivitet också praktiska tillämpningar inom områden som medicin, energiproduktion och miljöskydd. Därför är det ett viktigt ämne för studenter att lära sig om, både för dess inneboende intresse och för de många verkliga tillämpningar det har.
Praktiska tillämpningar av radioaktivitet
En av de vanligaste tillämpningarna av radioaktivitet är inom medicinområdet. Radioaktiva isotoper används i medicinska avbildningstekniker som PET- och SPECT-skanningar, vilket gör att läkare kan se inuti kroppen och diagnostisera sjukdomar. Radioaktiva isotoper används också i cancerbehandlingar, såsom strålterapi, där de används för att döda cancerceller.
Radioaktivitet används också i industrier som olje- och gasutforskning, där det används för att mäta genomsläppligheten hos bergformationer och flödet av vätskor genom dem. Radioaktiva isotoper används också i brandvarnare och i produktionen av självlysande klockor och instrument.
Sammanfattningsvis har radioaktivitet ett brett spektrum av tillämpningar inom områden som medicin, industri och även vardagliga konsumentprodukter. Det fortsätter att vara ett viktigt studieområde inom fysik och andra vetenskaper, och dess användning fortsätter att expandera när nya teknologier utvecklas.
Radioaktivitetsexperiment i skolor och universitet
Användningen av en geigermätare i ett radioaktivitetsexperiment möjliggör en mängd olika möjligheter. Genom att variera strålningsutsläppare och absorberare kan studenter observera effekterna av olika källor och material på de detekterade partikelsammanstötningarna. Detta kan hjälpa studenter att förstå radioaktivitetens egenskaper och beteendet hos olika partiklar.
Dessutom kan experiment som involverar bestämning av vilken typ av partikel som strålas ut genomföras genom att observera om partikeln absorberas eller inte. Genom att placera olika absorberare mellan källan och sonden kan studenterna bestämma de emitterade partiklarnas egenskaper och få en djupare förståelse för radioaktivitet.
Slutligen kan experiment som involverar bestämning av den geometriska formen av radioakivitetsutsläpp också genomföras med en geigermätare. Genom att noggrant mäta de detekterade partikelsammanstötningarna på olika avstånd kan studenter få insikter i den rumsliga fördelningen av radioaktivitet. Detta kan hjälpa studenter att förstå de grundläggande principerna för radioaktivitet och dess tillämpningar i verkligheten.
Potentiella lärandemål
Potentiella mål för aktiviteter som genomförs med laboratoriet är följande:
- Förstå egenskaperna och beteendet hos radioaktiva emissioner.
- Utföra experiment för att mäta effekterna av strålning på olika material.
- Bestämma typen av strålning som emitteras av en radioaktiv källa.
- Förstå principerna för strålningssäkerhet och hantering.
- Undersöka tillämpningar av radioaktivitet inom områden som medicin, industri och forskning.
- Förstå principerna för Geiger-mätare och deras användning vid mätning av radioaktivitet.
- Förstå den historiska utvecklingen av konceptet radioaktivitet och dess upptäckt.
- Utforska de etiska implikationerna av användningen av radioaktiva material.

Spektroskopi
Detta ultrakoncurrenta laboratorium är baserat på en experimentell övning om röntgenspektroskopi med hjälp av en apparat av märket LEYBOLD som är installerad i ett radiologiskt instrumentationslaboratorium vid National University of Costa Rica (Universidad Nacional de Costa Rica), som är beläget i byggnaden för tillämpad medicinsk fysik.
Utrustningen består av ett röntgenrör med en guld (Au) anod, tillsammans med en scintillationsdetektor konfigurerad med en förstärkare och en digitalisator som möjliggör bearbetning av information från mätningarna som gjorts av detektorn genom mjukvara.
Testet syftar till att karakterisera strålen från strålningskällan genom den experimentella beräkningen av spektrumet av röntgenstrålen som produceras i röret, samt att generera grundläggande uppfattningar om radiologisk instrumentering och hur variationen av dess parametrar används i industriella och medicinska tillämpningar.











