Obține acum acces la LCAL2003: Chemistry labs (ultraconcurrent)
Pentru doar:
9,99 USDO plată unică
6 luni de acces
Metode de plată acceptate:
- DigiKey (Nu este disponibil în fiecare țară)
- Card de credit sau debit
- PayPal
Trebuie să creezi sau să folosești un cont LabsLand pentru a continua.
Acces la distanță la 12 laboratoare incluse:
Încercați să cumpărați mai multe licențe pentru o clasă? Contactați-ne pentru reduceri pentru achiziții în volum
Ce este LabsLand?
LabsLand este rețeaua globală de laboratoare la distanță.
Echipamentul este întotdeauna real, nu o simulare.
Controlezi echipamentul real cu ajutorul camerelor web prin Internet.
Accesați acum. Nu este nevoie să așteptați trimiterea echipamentului.
Fără costuri ascunse: totul inclus. Fără costuri pentru accesorii sau transport.
Foarte ușor de utilizat: echipamentul funcționează deja.
Închiriază-l doar lunile de care ai nevoie pentru învățare.
Cum funcționează LabsLand?
LabsLand este o rețea globală de laboratoare reale disponibile online. Studenții (în școli, universități și platforme de învățare pe tot parcursul vieții) pot accesa laboratoarele reale prin Internet, folosind laptopul, tableta sau telefonul lor.
Laboratoarele sunt fie în timp real (Arduino, FPGA...) situate în diferite universități din întreaga lume. În anumite domenii (Fizică, Biologie, Chimie), laboratoarele sunt Laboratoare Ultraconcurente LabsLand, astfel încât universitatea a înregistrat toate combinațiile potențiale ale ceea ce se poate face în laborator (în unele cazuri, câteva mii) și le pune la dispoziție într-un mod interactiv.
În fiecare caz, laboratorul este întotdeauna real (nu simulat) și disponibil prin Web (nu este nevoie să obțineți hardware, să vă ocupați de livrare, etc.).
Verificați cum funcționează o sesiune tipică de utilizator în următorul video:
Titrare acid-bază II
Rezumat
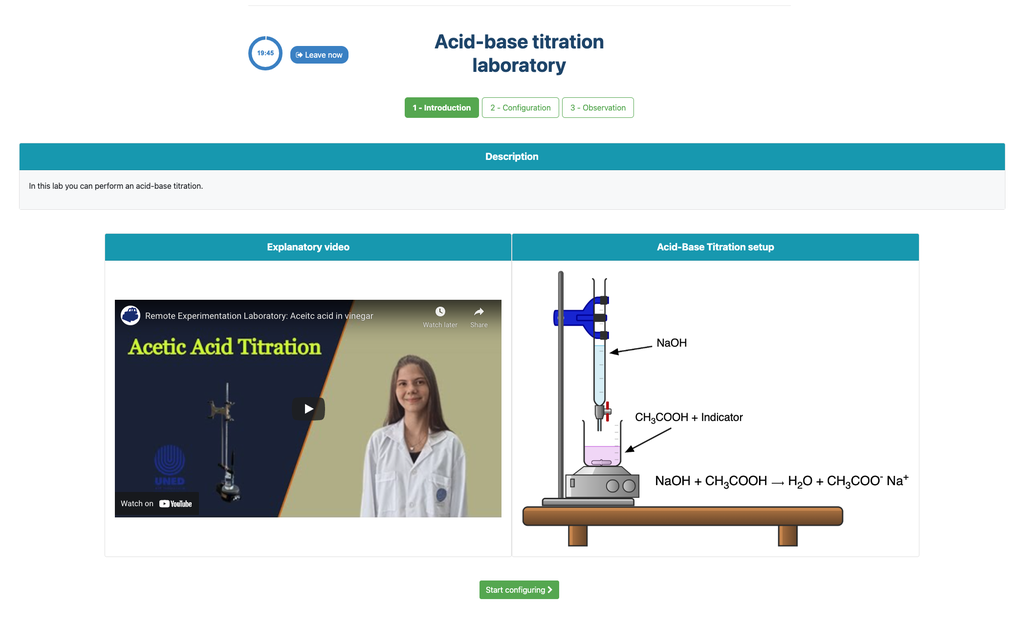
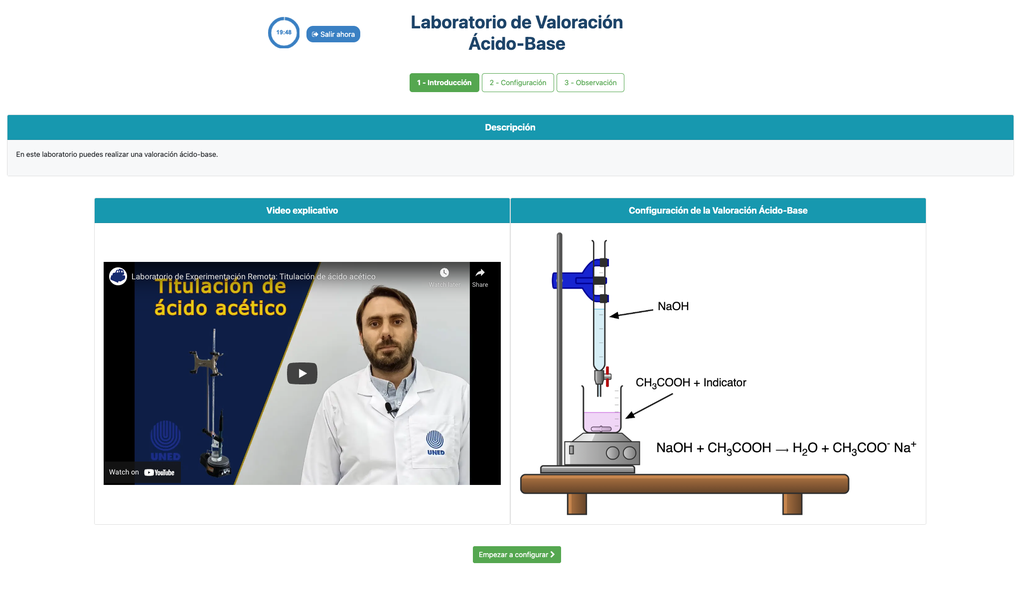
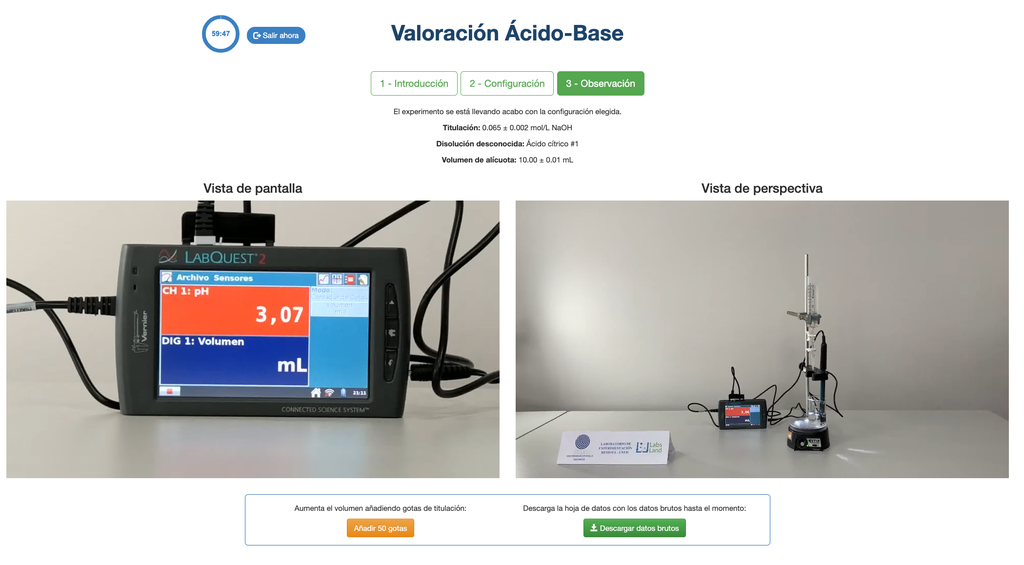
Efectuați o titrare acid-bază pentru a determina concentrația unei soluții necunoscute de acid acetic folosind un titrator cu hidroxid de sodiu. Acest laborator pune accent pe măsurători vizuale legate de meniscul biuretei și suportă două configurații diferite.
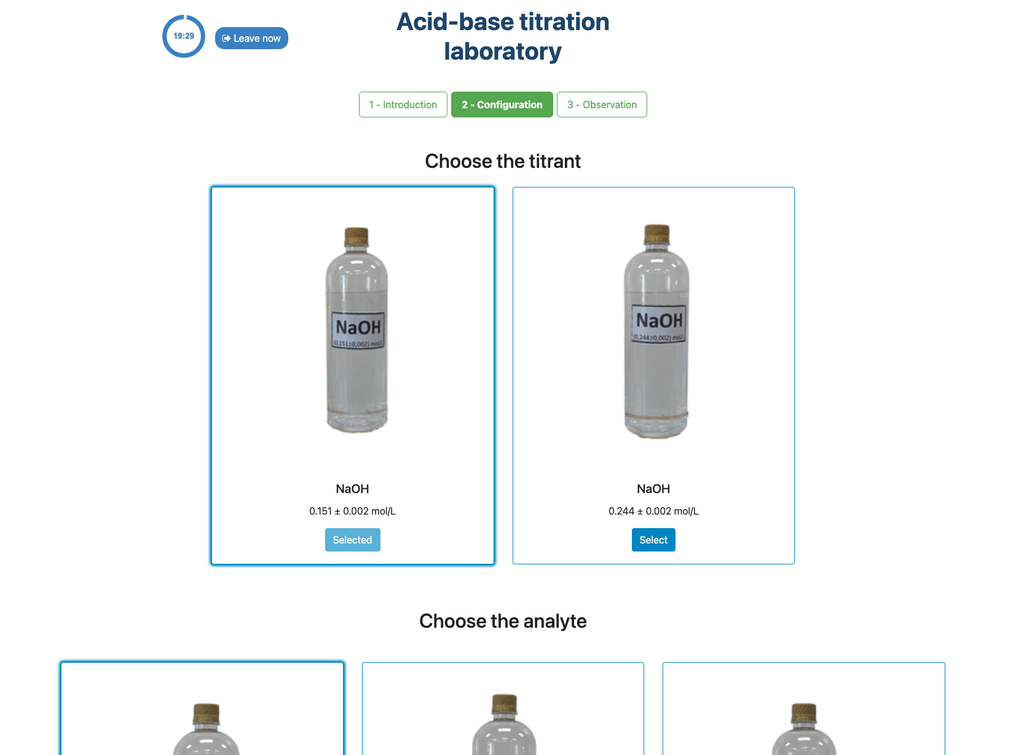
Prima este pentru o abordare potențiometrică: vei avea acces la un senzor de pH digital și îl poți folosi pentru a determina când soluția necunoscută a fost neutralizată.
A doua este pentru o abordare colorimetrică: te poți baza pe schimbarea de culoare datorită prezenței unui indicator fenolftaleinic, fără a avea un senzor de pH digital disponibil.
Titrare acid-bază
Titrările sunt o metodă volumetrică ce se bazează pe măsurarea cantității unui reactiv cu concentrație cunoscută (cunoscut ca standard primar) care este consumat de un eșantion cu concentrație necunoscută, cunoscut ca analizant.
Titrarea se desfășoară prin adăugarea titratorului la analizant folosind o biuretă, astfel încât să se obțină o substanță echivalentă chimic între titrator și analizant. Aceasta este cunoscută ca "punctul de echivalență" și este o valoare teoretică ce nu poate fi determinată experimental.
Estimarea experimentală a acestui punct este obținută printr-o aproximare cunoscută ca "punct final". Aceasta este determinată printr-o schimbare fizică. În acest caz, schimbarea culorii soluției se obține după adăugarea unei substanțe indicatoare: o substanță care își schimbă culoarea în anumite intervale de pH.
Pentru titrarea acid-bază folosim un indicator fenolftaleinic care devine roz deschis după un pH de aproximativ 8,4, care este o valoare foarte aproape de punctul de echivalență în cele mai comune titrări acid-bază.
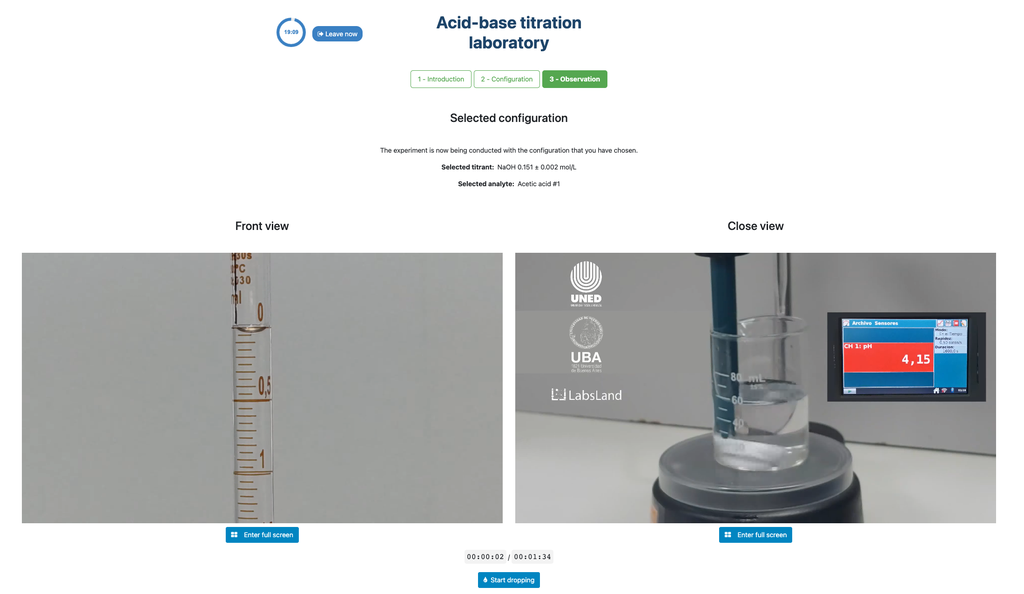
Alternativ, în configurația potențiometrică, un senzor de pH digital poate fi folosit pentru a determina "punctul de echivalență".
Abordare colorimetrică vs potențiometrică
Abordarea colorimetrică se bazează pe schimbarea de culoare oferită de indicatorul fenolftaleinic. Abordarea potențiometrică se bazează în schimb pe creșterea pH-ului măsurată de senzorul digital. În această versiune a laboratorului sunt disponibile două configurații diferite, una pentru fiecare abordare. În configurația colorimetrică, studenții s-ar putea să nu vadă senzorul de pH digital.
Diferențe cu laboratorul Titrare Acid-Bază II
În această versiune a laboratorului (Titrare Acid-Bază II) poți efectua titrarea acid-bază pentru o soluție necunoscută de acid acetic. În cealaltă versiune a laboratorului (vezi Titrare Acid-Bază I) poți efectua titrarea acid-bază pentru o soluție de acid citric în schimb.
Această versiune a laboratorului pune accent pe măsurători vizuale ale biuretei, incluzând citirea corectă a meniscului din biuretă. Cealaltă versiune a laboratorului (vezi Titrare Acid-Bază I) nu accentuează acest lucru și se concentrează în schimb pe calcul.
De asemenea, în această versiune poți alege între două configurații diferite: una pentru abordarea potențiometrică și una pentru abordarea colorimetrică. Configurația pentru abordarea colorimetrică nu arată senzorul de pH. În cealaltă versiune a laboratorului (vezi Titrare Acid-Bază I) există o singură configurație și senzorul este întotdeauna afișat.
Titrare acid-bază III
Rezumat
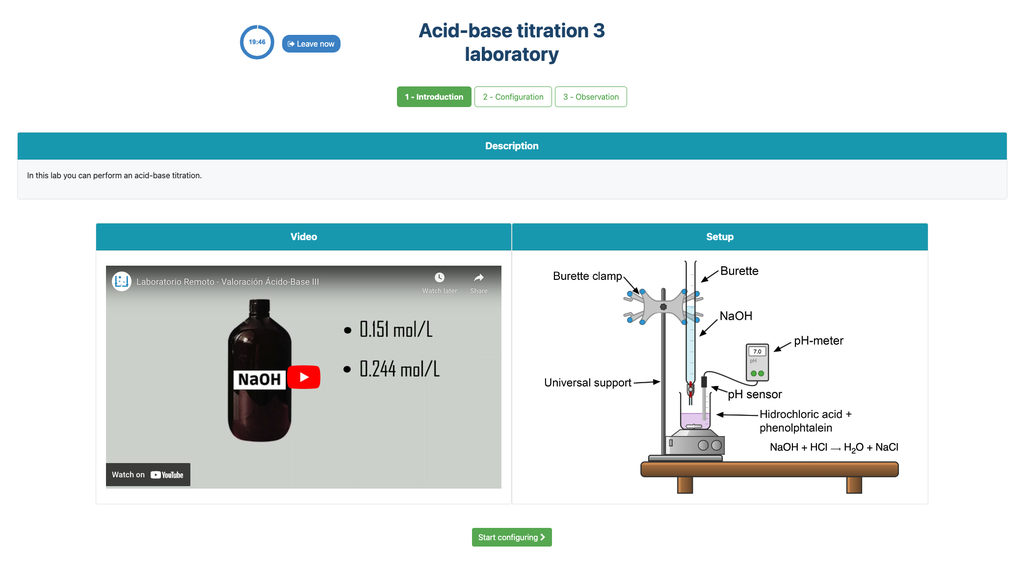
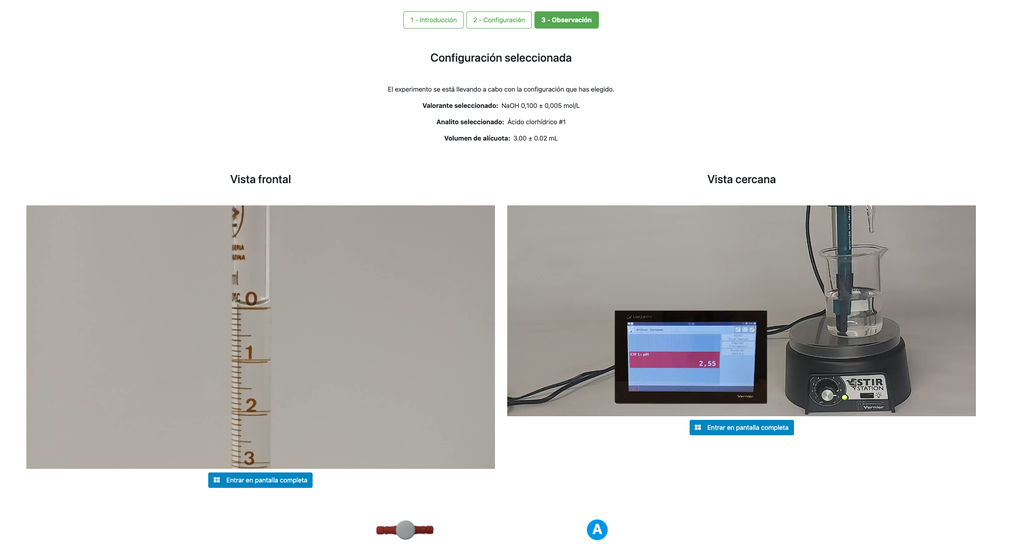
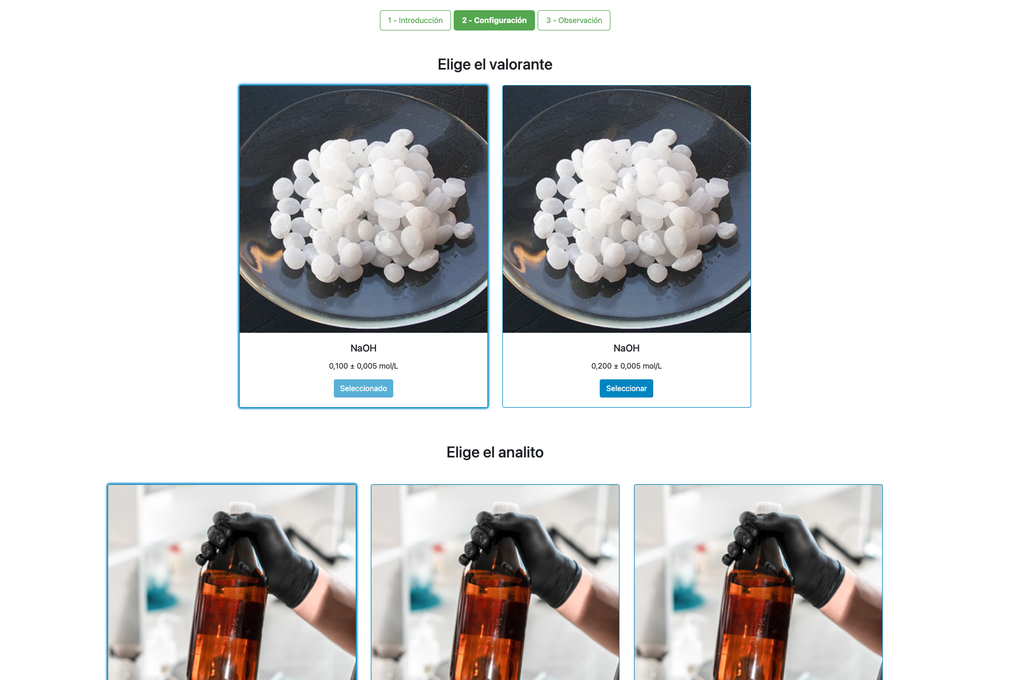
Efectuează o titrare acid-bază pentru a determina concentrația unei soluții necunoscute de acid clorhidric folosind un titrant de hidroxid de sodiu. Acest laborator pune accent asupra măsurătorilor vizuale care implică meniscul biuretei și susține două configurații diferite.
Prima este pentru o abordare potențiometrică: vei avea acces la un senzor digital de pH și îl poți folosi pentru a determina când soluția necunoscută a fost neutralizată.
A doua este pentru o abordare colorimetrică: te poți baza pe schimbarea culorii datorată prezenței unui indicator de fenolftaleină, fără să ai un senzor digital de pH disponibil.
Titrarea acid-bază
Titrările sunt o metodă volumetrică care se bazează pe măsurarea cantității unui reactant de concentrație cunoscută (cunoscut sub numele de standard primar) care este consumat de o mostră de concentrație necunoscută cunoscută ca analit.
Titrarea este efectuată prin adăugarea titrantului la analit folosind o biuretă, pentru a obține o substanță chimic echivalentă între titrant și analit. Acest punct este cunoscut ca „punctul de echivalență” și este o valoare teoretică care nu poate fi determinată experimental.
Estimarea experimentală a acestui punct este obținută printr-o aproximare cunoscută ca „punct final”. Acesta este determinat printr-o schimbare fizică. În acest caz, schimbarea culorii soluției este realizată după adăugarea unei substanțe indicator: o substanță care schimbă culoarea în anumite intervale de pH.
Pentru titrarea acid-bază folosim un indicator de fenolftaleină care devine roz deschis după un pH de aproximativ 8,4, care este o valoare foarte apropiată de punctul de echivalență în cele mai comune titrări acid-bază.
Alternativ, în configurația potențiometrică, un senzor digital de pH poate fi utilizat pentru a determina „punctul de echivalență”.
Abordare colorimetrică vs potențiometrică
Abordarea colorimetrică se bazează pe schimbarea de culoare oferită de indicatorul de fenolftaleină. Abordarea potențiometrică se bazează în schimb pe creșterea pH-ului măsurată de senzorul digital. În această versiune a laboratorului sunt disponibile două configurații diferite, câte una pentru fiecare abordare. În configurația colorimetrică, studenții nu pot vedea senzorul digital de pH.
Diferențe față de celelalte laboratoare de titrare
În această versiune a laboratorului (Titrarea Acid-Bază II) poți efectua titrarea acid-bază pentru o soluție necunoscută de acid clorhidric. În alte versiuni ale laboratorului poți efectua titrarea acid-bază pentru o soluție de acid citric (Titrarea Acid-Bază I) și acid acetic (Titrarea Acid-Bază II).
Atât această versiune a laboratorului (Titrarea Acid-Bază III), cât și Titrarea Acid-Bază II pun accent pe măsurătorile vizuale cu biureta, inclusiv citirea corectă a meniscului în biuretă. Cealaltă versiune a laboratorului (vezi Titrarea Acid-Bază I) nu pune accent pe aceasta, ci se concentrează pe calcule.
De asemenea, în aceste versiuni poți alege între două configurații diferite: una pentru abordarea potențiometrică și una pentru abordarea colorimetrică. Configurația pentru abordarea colorimetrică nu afișează senzorul de pH. În altă versiune a laboratorului (vezi Titrarea Acid-Bază I) există o singură configurație și senzorul este întotdeauna afișat.

Titrare acid-bază I
Rezumat
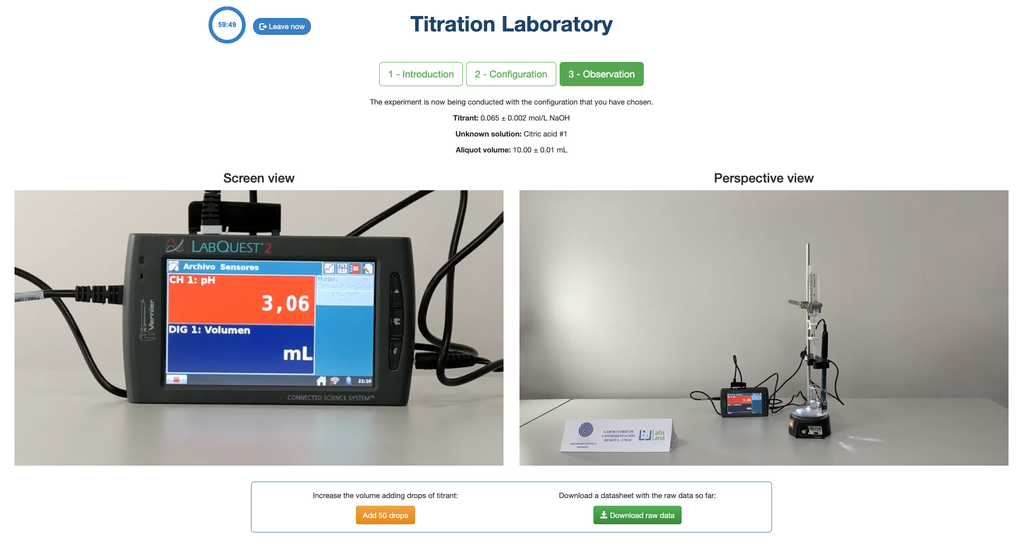
Realizați o titrare acid-bază pentru a determina concentrația unei soluții necunoscute de acid citric folosind un titrant de hidroxid de sodiu. Un senzor de pH digital este întotdeauna disponibil și un indicator fenolftaleină a fost aplicat soluției necunoscute, astfel încât să se poată utiliza atât o abordare potențiometrică, cât și colorimetrică. De asemenea, este disponibil un grafic în timp real.
Titrarea Acid-Bază
Titrările sunt o metodă volumetrică bazată pe măsurarea cantității unui reactiv de concentrație cunoscută (cunoscut sub numele de standard primar) care este consumat de un eșantion cu concentrație necunoscută cunoscut sub numele de analit.
Titrarea se realizează prin adăugarea titrantului la analit folosind o biuretă, astfel încât să se obțină o substanță chimică echivalentă între titrant și analit. Acest lucru este cunoscut sub numele de "punct de echivalență", și este o valoare teoretică care nu poate fi determinată experimental.
Estimarea experimentală a acestui punct se obține printr-o aproximație cunoscută sub numele de "punct final". Acesta este determinat printr-o schimbare fizică. În acest caz, schimbarea de culoare a soluției este realizată după adăugarea unei substanțe indicator: o substanță care își schimbă culoarea în anumite intervale de pH.
Pentru titrarea acid-bază, folosim un indicator fenolftaleină care devine roz pal după un pH de aproximativ 8,4, care este o valoare foarte apropiată de punctul de echivalență în cele mai comune titrări acid-bază.
Abordările Colorimetrică vs Potențiometrică
Abordarea colorimetrică se bazează pe schimbarea culorii oferite de indicatorul fenolftaleină. Abordarea potențiometrică se bazează pe ridicarea pH-ului măsurată de senzorul digital. În această versiune a laboratorului de titrare acid-bază se pot folosi ambele abordări. Senzorul digital este întotdeauna disponibil și nu poate fi ascuns.
Diferențe față de laboratorul Titrare Acid-Bază II
În această versiune a laboratorului (Titrare Acid-Bază I) puteți efectua titrarea acid-bază pentru o soluție necunoscută de acid citric. În cealaltă versiune a laboratorului (vezi Titrare Acid-Bază II) puteți efectua titrarea acid-bază pentru o soluție de acid acetic în schimb.
Această versiune a laboratorului subliniază calculele, dar nu are măsurători vizuale cu biureta printre obiectivele sale de învățare. Cealaltă versiune a laboratorului (vezi Titrare Acid-Bază II) subliniază măsurătorile vizuale, iar studenții trebuie să învețe să citească corect meniscul biuretei.
De asemenea, în această versiune există o singură experiență care poate fi folosită pentru ambele abordări colorimetrică și potențiometrică. În cealaltă versiune a laboratorului (vezi Titrare Acid-Bază II) sunt disponibile două configurații diferite, dintre care una ascunde senzorul digital astfel încât studenții să se poată baza doar pe schimbarea culorii.
Legea lui Boyle
Rezumat
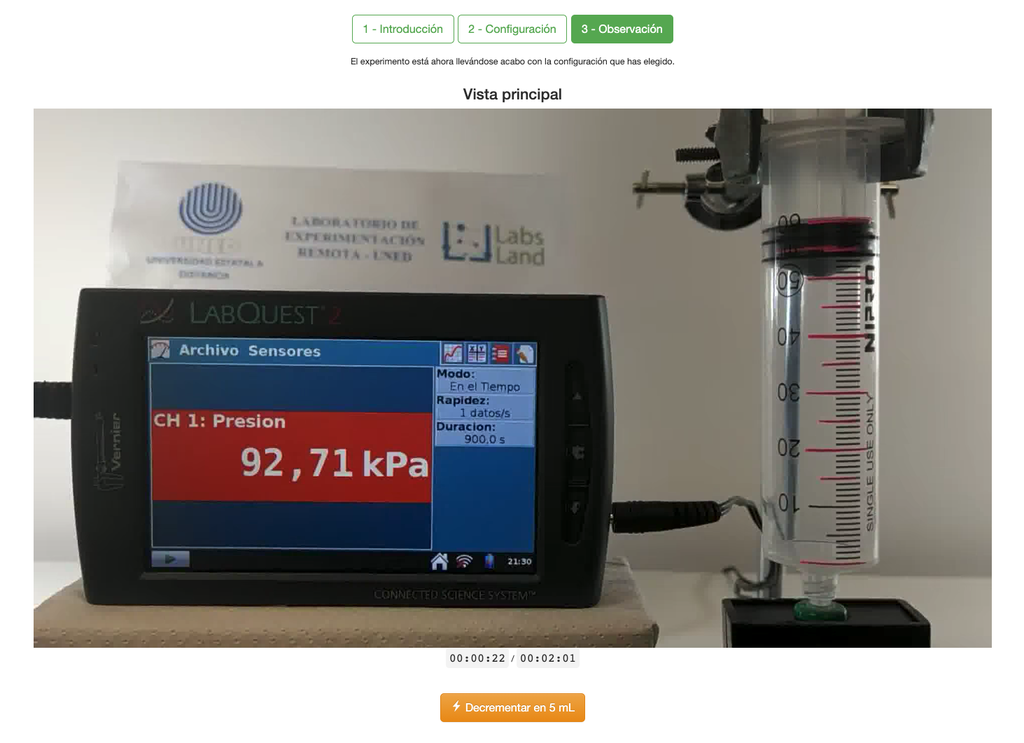
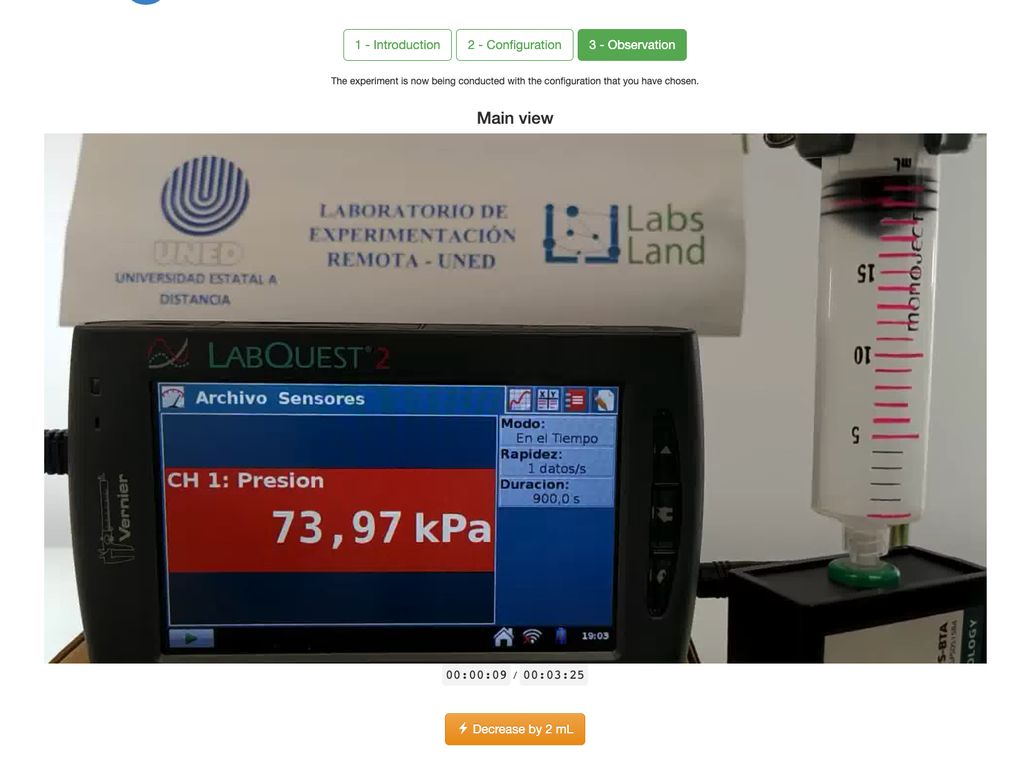
Laboratorul Legii lui Boyle permite elevilor să determine relația dintre presiunea și volumul unui gaz la o temperatură constantă și ambientală. Elevii pot alege din două seringi cu volum diferit și pot măsura presiunea gazului pe măsură ce reduc volumul. Experimentul este reflectat într-o analiză grafică sub forma unei izoterme. În acest mod, ei pot verifica Legea lui Boyle și pot învăța despre comportamentul gazelor într-un mod practic și accesibil.
Legea lui Boyle
Legea lui Boyle afirmă că la o temperatură constantă, volumul unui gaz este invers proporțional cu presiunea sa. Acest lucru înseamnă că atunci când presiunea unui gaz crește, volumul acestuia scade și invers. Legea lui Boyle poate fi exprimată matematic ca:
V 1/P
Unde V este volumul gazului și P este presiunea gazului.
Laboratorul Legii lui Boyle permite elevilor să pună în practică această lege și să o verifice într-un context experimental. Măsurând volumul și presiunea gazului la momente diferite, ei pot trasa un grafic izoterm care arată cum volumul gazului se schimbă în funcție de presiunea sa. Dacă graficul izoterm este în concordanță cu Legea lui Boyle, atunci elevii au verificat experimental legea.
Realizarea unor astfel de experimente este un mod excelent de a învăța despre comportamentul gazelor și despre cum sunt legate diferitele variabile. În plus, experimentele practice pot fi mai accesibile și mai memorabile pentru elevi decât simpla citire despre lege într-un manual. Graficul izoterm vizualizează clar comportamentul gazului și verifică dacă predicțiile Legii lui Boyle sunt îndeplinite.
Aplicarea în Educația Secundară și Universitară
Laboratorul Legii lui Boyle este, de obicei, aplicat în cursurile de știință la nivel de liceu și în cursurile de chimie la nivel universitar. La nivel de liceu, laboratorul poate fi aplicat într-un curs de știință unde sunt studiate conceptele de bază ale chimiei și fizicii, cum ar fi presiunea și volumul gazelor. La universitate, laboratorul Legii lui Boyle poate fi aplicat într-un curs de chimie mai avansat, unde este aprofundat studiul gazelor și al comportamentului acestora.
Obiective
Un laborator al Legii lui Boyle poate avea diferite obiective educaționale în funcție de nivelul educațional la care este aplicat. Iată câteva exemple de obiective pe care le poate avea un laborator al Legii lui Boyle la nivel liceal și universitar:
La nivel liceal:
- Elevii înțeleg Legea lui Boyle și importanța sa în fizica gazelor.
- Elevii își exersează abilitățile experimentale și de observare.
- Elevii își dezvoltă abilitățile de analiză și reprezentare a datelor.
- Elevii înțeleg relația dintre temperatură, presiune și volumul gazelor.
La nivel universitar:
- Studenții cunosc Legea lui Boyle și importanța sa în fizica gazelor.
- Studenții demonstrează abilități experimentale și de observare în laborator.
- Studenții aplică conceptele teoretice ale fizicii gazelor în situații practice.
- Studenții își dezvoltă abilitățile de analiză și reprezentare a datelor într-un context științific.
- Studenții înțeleg cum se relaționează temperatura, presiunea și volumul gazelor în diferite situații.
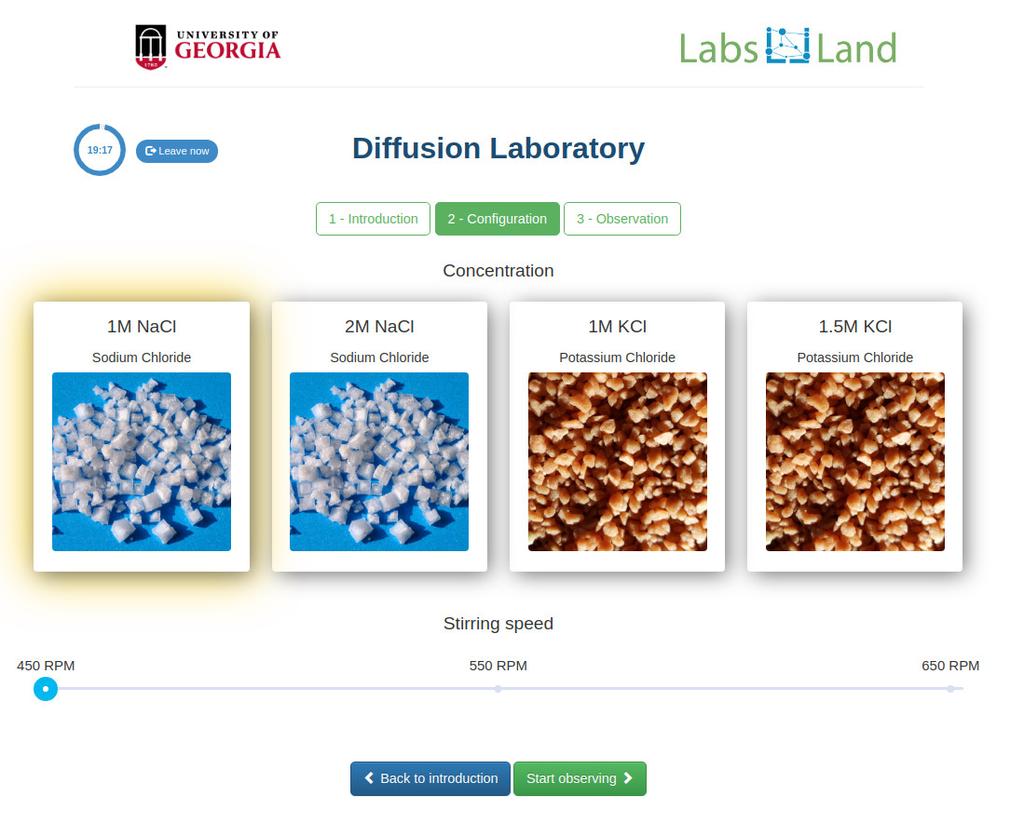
Diffusion laboratory - basic
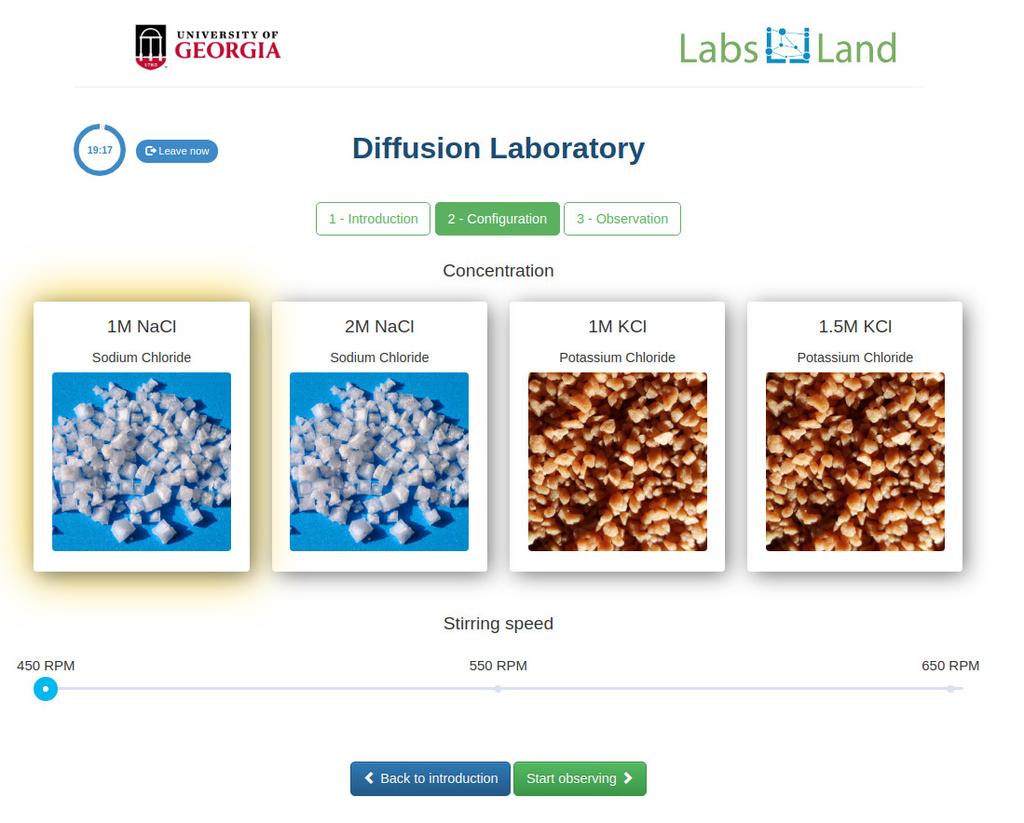
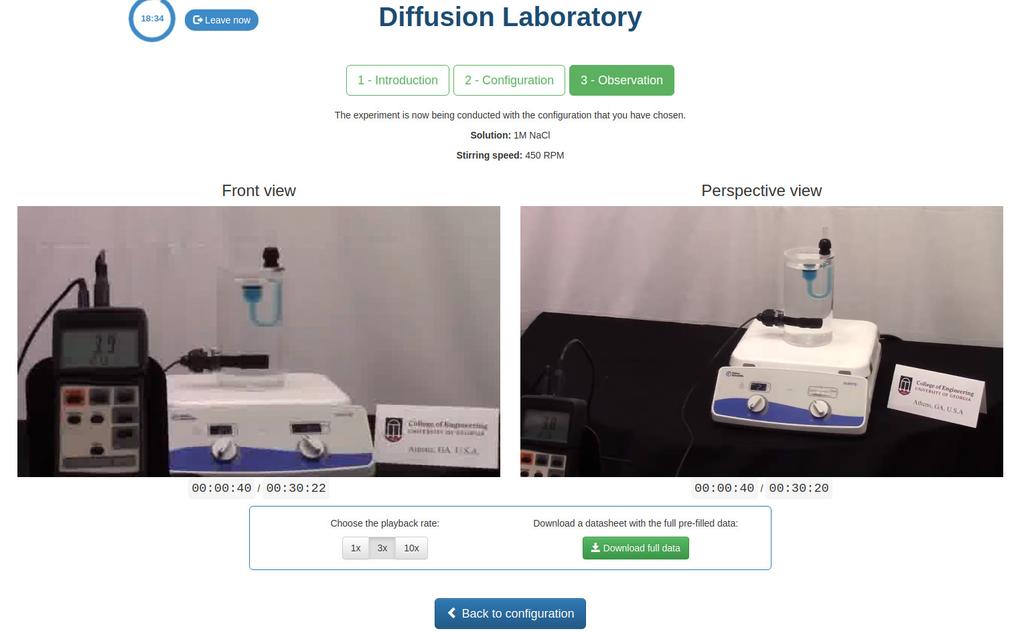
Diffusion laboratory - data
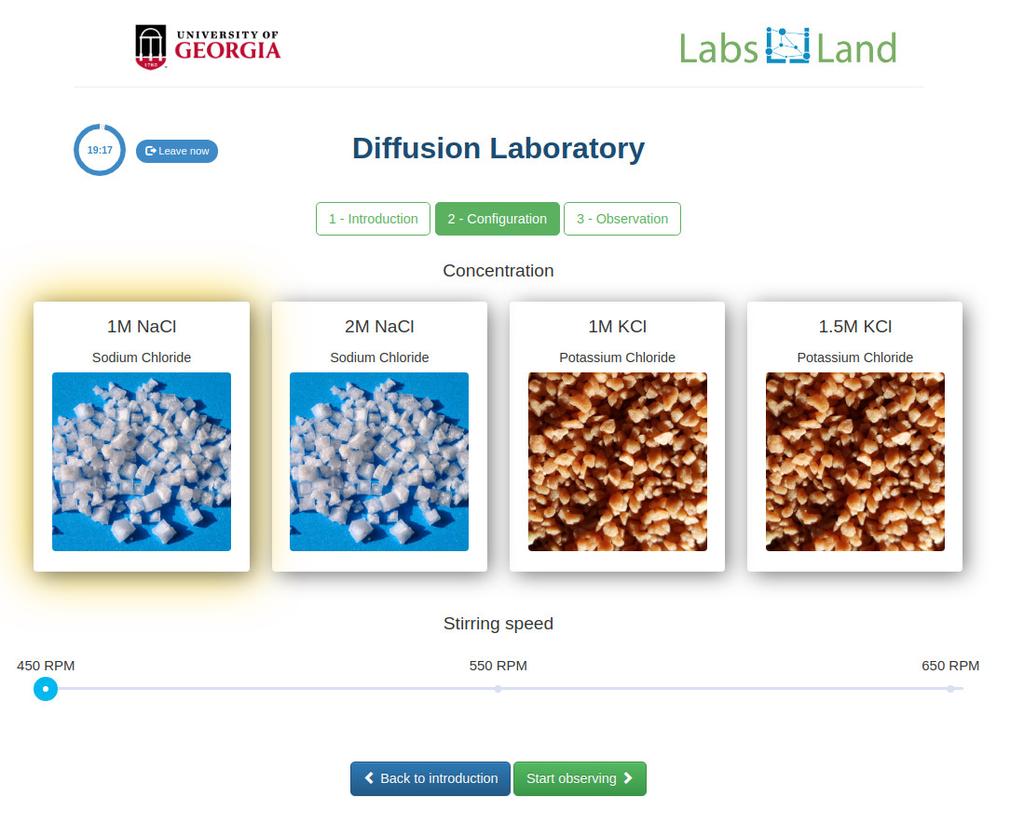
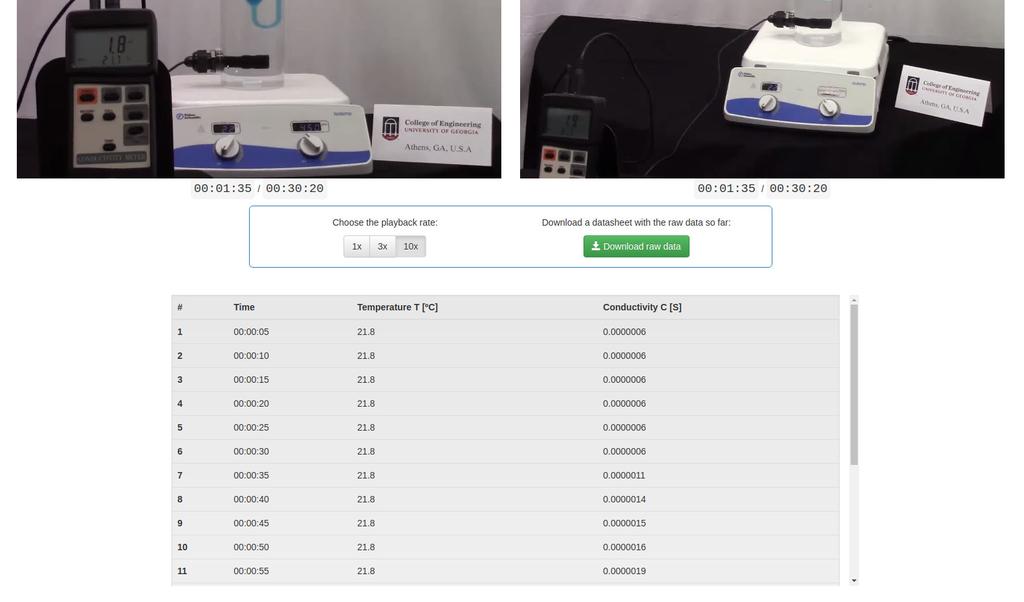
Diffusion laboratory - full
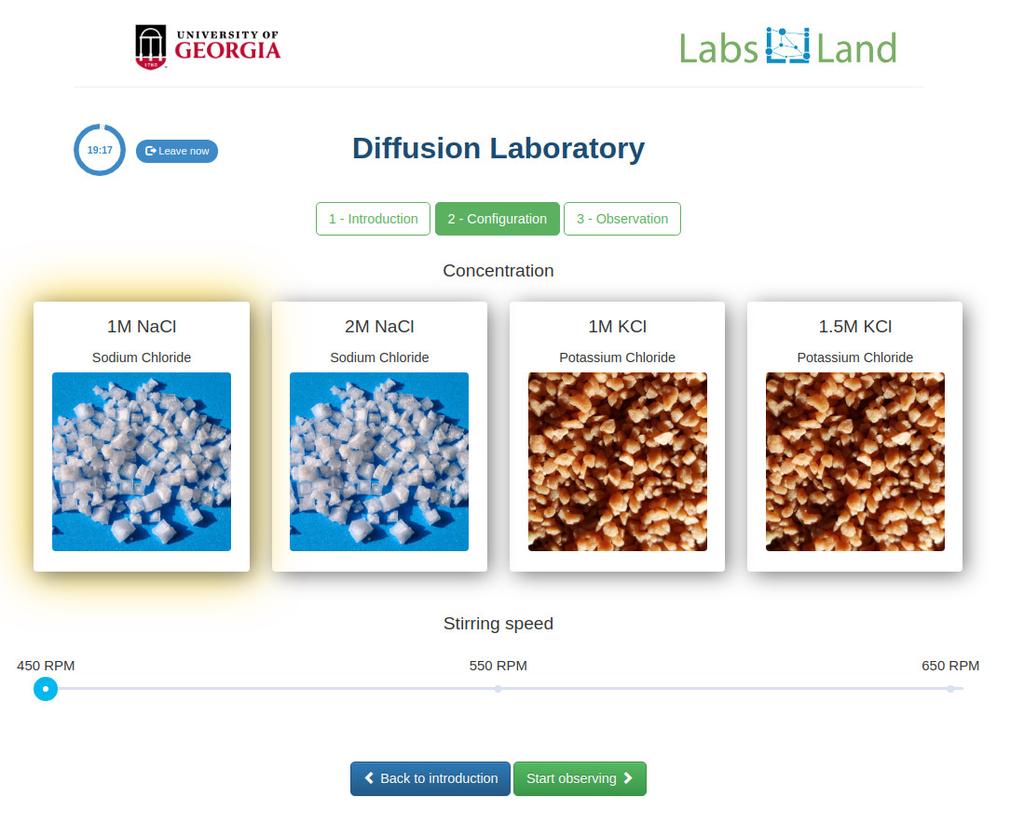
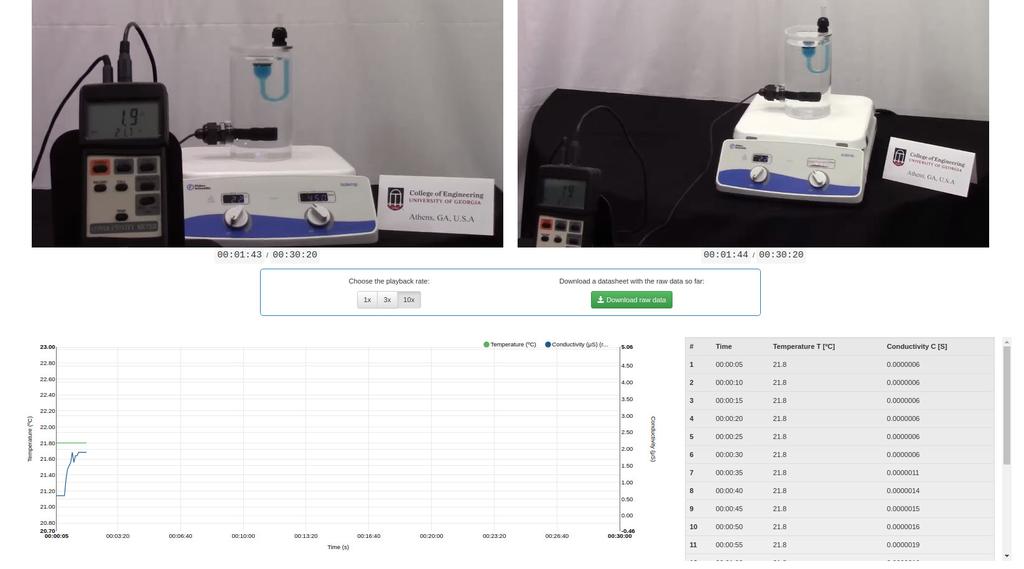
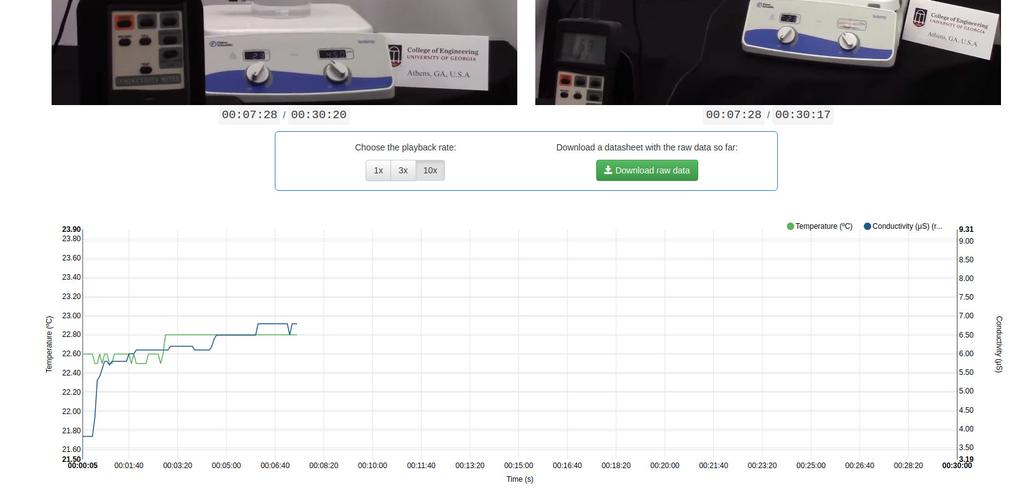
Diffusion laboratory - plot
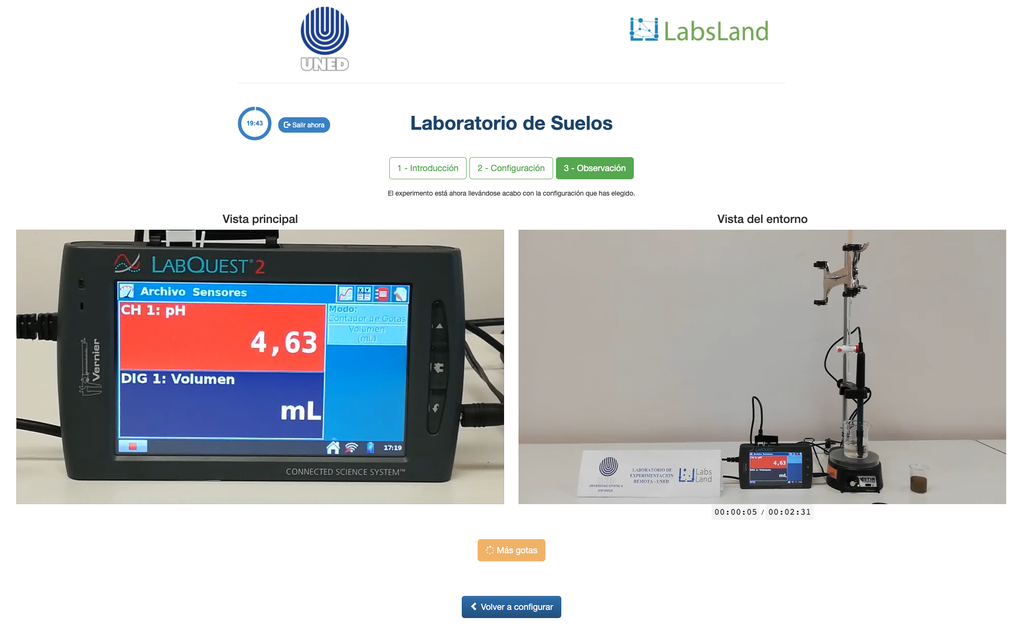
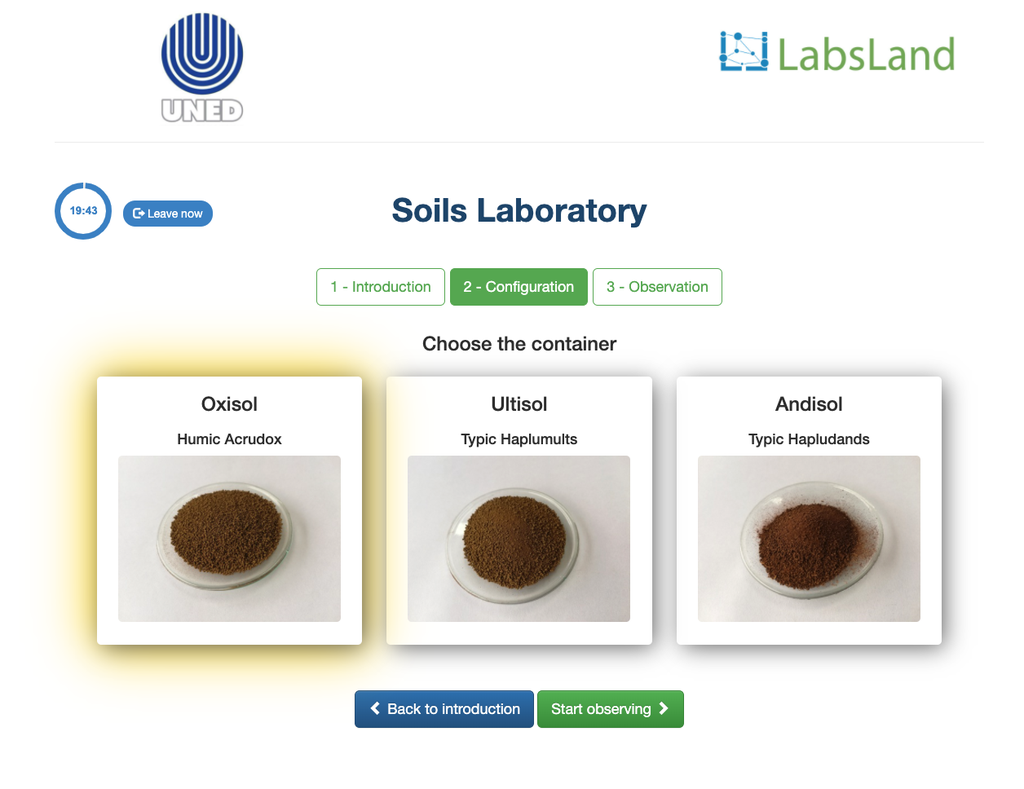
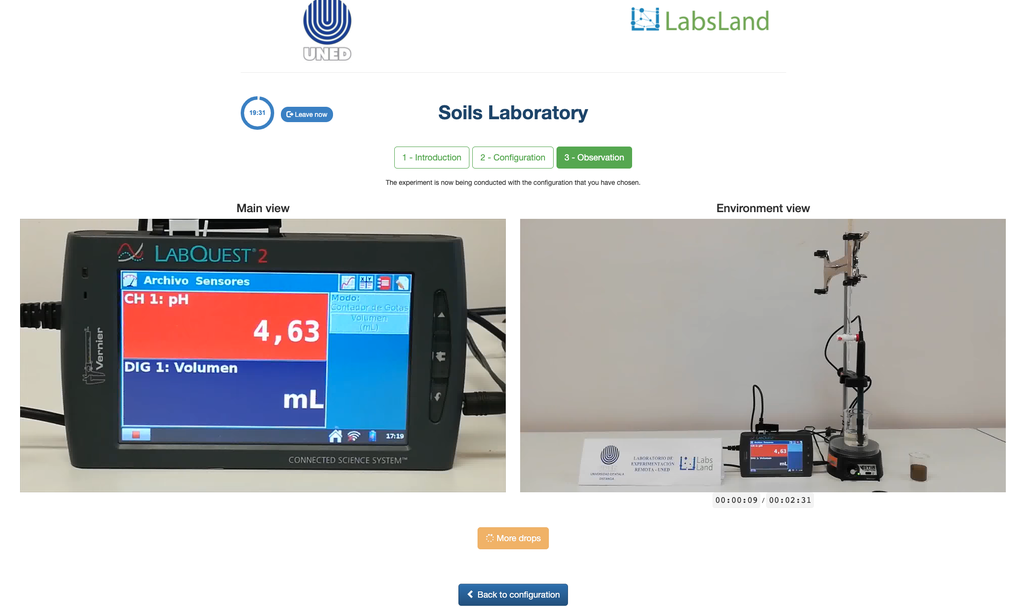
Aciditatea schimambabilă a solurilor
Aciditatea solurilor poate apărea din cauza diferitelor procese care promovează o reducere a pH-ului. Aceste procese apar în mod natural sau prin acțiunea umană. Principalele surse de aciditate a solului sunt asociate cu ionii de hidrogen (H+) și ionii de aluminiu (Al+3) din soluția solului. Aciditatea schimbabilă este determinată prin utilizarea soluțiilor de săruri neutre, cum ar fi clorura de potasiu (KCl). Ionii acizi (aluminiu și hidroniu) care sunt reținuți în fracția coloidală a solului, în prezența unui ion de dislocare (K+), fac ca aceștia să intre în soluția solului. Ulterior, acea soluție este titrată cu o soluție de hidroxid de sodiu de concentrație exactă pentru a atinge ultimul punct al reacției de neutralizare, folosind fenolftaleina ca indicator.

Legea lui Gay-Lussac
Legea lui Gay-Lussac ne permite să studiem comportamentul gazelor și este adesea studiată în fizică și chimie. Ea relaționează presiunea unui gaz cu temperatura sa, în timp ce alți parametri precum volumul și cantitatea rămân constante.
Există diverse moduri de a verifica legea lui Gay-Lussac. În acest experiment vom verifica că, pentru o cantitate dată de gaz, presiunea este direct proporțională cu temperatura.
Radioactivitate
Sumar
Setup-ul, util pentru școli și universități, include un detector Geiger care poate măsura numărul de coliziuni de particule detectate. Utilizatorul poate alege dintre diferite surse radioactive, precum și un absorbant de plasat între sursa radioactivă și sonda. În plus, alți parametri pe care utilizatorii îi pot varia sunt distanța și numărul de teste. Acest lucru permite o gamă largă de experimente și oportunități de învățare.
Radioactivitate
Radioactivitatea este procesul în care un nucleu atomic își pierde energia prin emiterea de particule și radiații. Acest lucru poate apărea în mod natural în anumite elemente sau artificial prin utilizarea reacțiilor nucleare. În contextul fizicii la școli și universități, studiul radioactivității poate oferi perspective valoroase asupra naturii fundamentale a materiei și legilor fizicii.
Un experiment comun în acest domeniu este măsurarea radioactivității folosind un detector Geiger. Acest instrument este capabil să detecteze emisia de particule de la o sursă radioactivă, permițând elevilor să înțeleagă principiile de bază ale radiației și efectele acesteia asupra materiei. Variind tipul de sursă radioactivă, distanța dintre sursă și detector și tipul de material absorbant plasat între cele două, elevii pot explora o gamă largă de fenomene și pot obține o înțelegere mai profundă a principiilor subadiacente.
Pe lângă valoarea sa educațională, studiul radioactivității are, de asemenea, aplicații practice în domenii precum medicina, producția de energie și protecția mediului. Prin urmare, este un subiect important de învățat pentru studenți, atât pentru interesul său intrinsec, cât și pentru numeroasele aplicații reale pe care le are.
Aplicații reale ale radioactivității
Una dintre cele mai comune aplicații ale radioactivității este în domeniul medicinei. Izotopii radioactivi sunt utilizați în tehnici de imagistică medicală, cum ar fi scanările PET și SPECT, care permit medicilor să vadă în interiorul corpului și să diagnosticheze boli. Izotopii radioactivi sunt de asemenea utilizați în tratamentele pentru cancer, cum ar fi radioterapia, unde sunt utilizați pentru a distruge celulele canceroase.
Radioactivitatea este de asemenea utilizată în industrii precum explorarea petrolului și a gazului, unde este folosită pentru a măsura permeabilitatea formațiunilor de rocă și fluxul de fluide prin acestea. Izotopii radioactivi sunt de asemenea folosiți în detectoarele de fum și în producția de ceasuri și instrumente luminoase.
În general, radioactivitatea are o gamă largă de aplicații în domenii precum medicina, industria și chiar produsele de consum zilnice. Continuă să fie un domeniu important de studiu în fizică și alte științe, iar utilizările sale continuă să se extindă odată cu dezvoltarea noilor tehnologii.
Experimente de radioactivitate în școli și universități
Utilizarea unui detector Geiger într-un experiment de radioactivitate permite o gamă largă de posibilități. Variind emitenții și absorbanții de radiație, elevii pot observa efectele diferitelor surse și materiale asupra coliziuniilor de particule detectate. Acest lucru poate ajuta elevii să înțeleagă proprietățile radioactivității și comportamentul diferitelor particule.
În plus, experimentele care implică determinarea tipului de particule radiate pot fi realizate prin observarea dacă particula este sau nu absorbită. Prin plasarea diferiților absorbanți între sursă și sondă, elevii pot determina proprietățile particulelor emise și pot obține o înțelegere mai profundă a radioactivității.
În cele din urmă, experimentele care implică determinarea formei geometrice a emisiilor de radioactivitate pot fi de asemenea realizate utilizând un detector Geiger. Prin măsurarea atentă a coliziuniilor de particule detectate la diferite distanțe, elevii pot obține perspective asupra distribuției spațiale a radioactivității. Acest lucru poate ajuta elevii să înțeleagă principiile fundamentale ale radioactivității și aplicațiile sale în lumea reală.
Obiective potențiale de învățare
Obiective potențiale ale activităților realizate cu laboratorul sunt următoarele:
- Înțelegerea proprietăților și comportamentului emisiilor radioactive.
- Realizarea de experimente pentru a măsura efectele radiației asupra diferitelor materiale.
- Determinarea tipului de radiație emisă de o sursă radioactivă.
- Înțelegerea principiilor siguranței și manipulării radiațiilor.
- Investigarea aplicațiilor radioactivității în domenii precum medicina, industria și cercetarea.
- Înțelegerea principiilor detectoarelor Geiger și utilizarea lor în măsurarea radioactivității.
- Înțelegerea dezvoltării istorice a conceptului de radioactivitate și descoperirea sa.
- Explorarea implicațiilor etice ale utilizării materialelor radioactive.

Spectroscopie
Acest laborator ultraconcurent se bazează pe o practică experimentală despre spectroscopia cu raze X folosind un dispozitiv marca LEYBOLD care este instalat într-un laborator de instrumentație radiologică din Universitatea Națională din Costa Rica (Universidad Nacional de Costa Rica), situată în clădirea Fizicii Medicale Aplicate.
Montajul constă dintr-un tub de raze X cu anod de aur (Au), împreună cu un detector de scintilație configurat cu un preamplificator și un digitalizator care permite procesarea informațiilor din măsurătorile efectuate de detector prin software.
Testul își propune să caracterizeze fasciculul sursei de radiație prin calculul experimental al spectrului fasciculului de raze X produs în tub, pe lângă generarea de noțiuni de bază despre instrumentația radiologică și cum este utilizată variația parametrilor săi în aplicațiile industriale și medicale.











